题目内容
燃料电池的突出优点是把化学能直接转变为电能,而不经过热能中间形式,现已广泛使用.如甲烷燃料电池,其电极反应为:负极:CH4+10OH--8e-=CO32-+7H2O正极:2O2+8e-+4H2O=8OH-.今欲得27g水,则电池中电子转移的物质的量为( )
分析:先根据电极反应式写出电池反应式,再根据水和转移电子的关系式计算.
解答:解:CH4+10 OH--8e-=CO32-+7H2O ①
2O2+8e-+4H2O=8OH-. ②
将方程式①+②得 CH4 +2OH-+2O2=3H2O+CO32-转移电子
(3×18)g 8mol
27g 4mol
故选C
2O2+8e-+4H2O=8OH-. ②
将方程式①+②得 CH4 +2OH-+2O2=3H2O+CO32-转移电子
(3×18)g 8mol
27g 4mol
故选C
点评:本题以原电池为载体考查了方程式的有关计算,两电极上电极反应式相加即得电池反应方程式,要注意得失电子数相等时才能相加,得出电池反应方程式是解本题的关键.

练习册系列答案
相关题目
燃料电池的突出优点是将化学能直接转变为电能,而不经过热能这一中间环节,能量利用率高,已应用于宇宙飞船、航空站及潜水中.氢氧燃料电池可同时供应电和水蒸气,所用燃料为H2,电解质为熔融的K2CO3.已知该电池的正极反应为:O2+2CO2+4e-?2CO32-.下列叙述正确的是( )
| A、放电时CO32-向正极移动 | B、放电时OH-向负极移动 | C、负极反应为H2+CO32--2e-?H2O+CO2 | D、当该电池产生的水蒸气折算成标准状况下的体积为22.4L时,转移电子4mol |
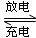 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是
(填序号)
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是
(填序号) 则负极反应式为___ ____________ _
_,正极反应式为
。一段时间后,KOH溶液的浓度
(填“变大”、“变小”或“不变”)
则负极反应式为___ ____________ _
_,正极反应式为
。一段时间后,KOH溶液的浓度
(填“变大”、“变小”或“不变”)