题目内容
有甲、乙、丙三种元素,甲元素M层的电子数是其K层的电子数的
,乙元素原子核内无中子,丙元素原子核内有8个质子.
(1)写出丙元素的元素符号 ,画出丙的原子结构示意图 ;
(2)写出乙元素的三种核素符号分别为 、 、 ;
(3)乙、丙两种元素形成的具有18电子的化合物是 .(填化学式)
(4)写出甲、乙、丙三种元素组成的化合物在水中的电离方程式 .
| 1 |
| 2 |
(1)写出丙元素的元素符号
(2)写出乙元素的三种核素符号分别为
(3)乙、丙两种元素形成的具有18电子的化合物是
(4)写出甲、乙、丙三种元素组成的化合物在水中的电离方程式
考点:原子结构与元素的性质
专题:元素周期律与元素周期表专题
分析:甲元素M层的电子数是其K层的电子数的
,M层电子数为1,则甲为Na;乙元素原子核内无中子,则乙为H元素;丙元素原子核内有8个质子,则丙为O元素,据此解答.
| 1 |
| 2 |
解答:
解:甲元素M层的电子数是其K层的电子数的
,M层电子数为1,则甲为Na;乙元素原子核内无中子,则乙为H元素;丙元素原子核内有8个质子,则丙为O元素,
(1)丙元素的元素符号为O,丙的原子结构示意图为,故答案为:O;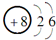 ;
;
(2)乙为H元素,其三种核素符号分别为11H、21H、31H,故答案为:11H;21H;31H;
(3)乙、丙两种元素形成的具有18电子的化合物是H2O2,故答案为:H2O2;
(4)甲、乙、丙三种元素组成的化合物为NaOH,在水中的电离方程式为:NaOH═Na++OH-,故答案为:NaOH═Na++OH-.
| 1 |
| 2 |
(1)丙元素的元素符号为O,丙的原子结构示意图为,故答案为:O;
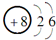 ;
;(2)乙为H元素,其三种核素符号分别为11H、21H、31H,故答案为:11H;21H;31H;
(3)乙、丙两种元素形成的具有18电子的化合物是H2O2,故答案为:H2O2;
(4)甲、乙、丙三种元素组成的化合物为NaOH,在水中的电离方程式为:NaOH═Na++OH-,故答案为:NaOH═Na++OH-.
点评:本题考查原子结构、常用化学用语,比较基础,有利于基础知识的巩固.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
下列说法不正确的是( )
| A、乙烯可作水果的催熟剂 |
| B、硅胶可作袋装食品的干燥剂 |
| C、福尔马林可作食品的保鲜剂 |
| D、小苏打可作胃酸的中和剂 |
元素X、Y和Z可结合形成化合物XYZ3;X、Y和Z的原子序数之和为26;Y和Z在同一周期.下列有关推测正确的是( )
| A、XYZ3是一种可溶于水的酸,且X与Y可形成共价化合物XY |
| B、XYZ3是一种微溶于水的盐,且Y与Z可形成共价化合物化合物YZ或YZ2 |
| C、XYZ3是一种易溶于水的盐,且X与Z可形成离子化合物XZ |
| D、XYZ3是一种离子化合物,且Y与Z可形成离子化合物YZ3 |
剧毒的氰化物可与碱发生反应2CN-+8OH-+5C12═2CO2+N2+10C1-+4H2O下列判断正确的是( )
| A、当有0.2 mol CO2生成时,溶液中阴离子的物质的量增加l mol |
| B、该反应中,每有2mol CN-反应,转移电子为10 mol |
| C、上述反应中的还原剂是OH- |
| D、还原性:Cl->CN- |
3Cl2+8NH3=6NH4Cl+N2的反应中,被氧化的NH3与未被氧化的NH3的分子数之比为( )
| A、1:6 | B、3:1 |
| C、1:3 | D、6:1 |
设NA代表阿伏加德罗常数,下列说法不正确的是( )
| A、阿伏加德罗常数NA是0.012 kg C-12中所含的原子数 |
| B、1 g氢气所含氢原子数目为NA |
| C、22.4 L H2O分子中氢原子与氧原子个数比为2:1 |
| D、1 mol?L-1 NaOH溶液中所含有的Na+离子数目为NA |
下列物质水溶液能导电,但是属于非电解质的是( )
| A、NH3 |
| B、(NH4)2SO4 |
| C、Cl2 |
| D、Na2O |