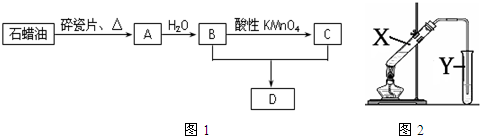
题目内容
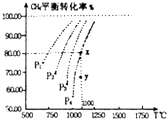 在一恒容的密闭窗口中充入0.1mol/LCO2,0.1mol/L CH4,在一定条件下发生反应:CH4(g)+CO2(g)?2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是( )
在一恒容的密闭窗口中充入0.1mol/LCO2,0.1mol/L CH4,在一定条件下发生反应:CH4(g)+CO2(g)?2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是( )| A、上述反应的△H<0 |
| B、压强:P4>P3>P2>P1 |
| C、1100℃时该反应平衡常数为1.64 |
| D、压强为P4时,在y点:V正>V逆 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、随温度的升高转化率增大;
B、增大压强,平衡向气体体积减小的方向移动;
C、利用三段式计算出平衡时的浓度求算;
D、y点时甲烷的转化率小,平衡正向移动.
B、增大压强,平衡向气体体积减小的方向移动;
C、利用三段式计算出平衡时的浓度求算;
D、y点时甲烷的转化率小,平衡正向移动.
解答:
解:A、从图象分析,随温度升高转化率增大,正反应吸热,△H>0,故A错误;
B、压强增大,平衡向逆反应方向移动,甲烷的转化率变小,故P4>P3>P2>P1,故B正确;
C、反应 CH4(g)+CO2(g)?2CO(g)+2H2(g),
起始(mol/L) 0.1 0.1 0 0
变化(mol/L) 0.08 0.08 0.16 0.16
平衡(mol/L) 0.02 0.02 0.16 0.16
平衡常数K=
=1.64,故C正确;
D、在y点,甲烷的转化率小于平衡时的转化率,平衡正向移动,V正>V逆,故D正确.
故选A.
B、压强增大,平衡向逆反应方向移动,甲烷的转化率变小,故P4>P3>P2>P1,故B正确;
C、反应 CH4(g)+CO2(g)?2CO(g)+2H2(g),
起始(mol/L) 0.1 0.1 0 0
变化(mol/L) 0.08 0.08 0.16 0.16
平衡(mol/L) 0.02 0.02 0.16 0.16
平衡常数K=
| 0.162×0.162 |
| 0.02×0.02 |
D、在y点,甲烷的转化率小于平衡时的转化率,平衡正向移动,V正>V逆,故D正确.
故选A.
点评:本题考查了平衡受温度、压强的影响而移动的问题,注意看准图象是解题的关键,难度中等.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、煤焦油中含有苯、二甲苯、苯酚等化工原料 |
| B、石油裂解的主要目的是为了获得短链不饱和烃 |
| C、烟、雾属于胶体,能产生丁达尔效应 |
| D、可用热的饱和碳酸钠溶液除去金属表面的矿物油 |
下列有关物质的性质或应用的说法不正确的是( )
| A、制水泥和玻璃都用石灰石作原料 |
| B、硫和氮的氧化物大量排放都可能引起酸雨 |
| C、二氧化硅是光纤制品的主要化学成分 |
| D、食用加碘盐可防治核辐射对人体的伤害 |
用a、b两个惰性电极电解0.2L一定浓度的硫酸铜溶液,当a极上产生4.48L(标况)气体时,b极上只有固体析出.然后将电源反接,当b极产生4.48L(标况)气体时,溶液质量共减少45.4克.下列说法正确的是( )
| A、将电源反接前a极发生的反应为:2H++2e-=H2↑ |
| B、将电源反接后,a极发生的反应只有Cu2++2 e-=Cu |
| C、整个电解过程只产生一种气体 |
| D、原硫酸铜溶液的浓度为2.5mol/L |
在水中加入下列物质,可使水的电离平衡向右移动的是( )
| A、硫酸 | B、氢氧化钾 |
| C、氯化铁 | D、硝酸钡 |
下列物质混合后溶液中溶质的质量分数最大的是( )
| A、4.6g钠投入45.4g水中 |
| B、6.2g氧化钠投入42.2g水中 |
| C、7.8g过氧化钠投入42.2g水中 |
| D、8g烧碱投入42g水中 |
漂白粉在溶液中存在下列平衡:ClO-+H2O?HClO+OH-,下列措施能提高其漂白性能的是( )
| A、加水稀释 |
| B、加少量NaOH |
| C、加适量氢碘酸 |
| D、通入CO2 |