题目内容
4.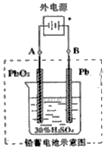 铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等.回答下列问题:
铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等.回答下列问题:(1)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为PbO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$PbCl2+Cl2↑+2H2O.
(2)铅蓄电池是典型的二次电池,它的正负极格板是惰性材料,电池总反应式为:
①放电时:负极的电极反应式是Pb-2e-+SO42-=PbSO4 ;
②当外电路通过2mol电子时,消耗硫酸2mol.
(3)PbO2可以通过石墨为电极,Pb(NO3)2和Cu(NO3)2的混合溶液为电解液电解制取.阳极析出的物质是PbO2,阴极上观察到的现象是石墨电极底部有红色物质附着;若电解液中不加入Cu(NO3)2,阳极发生的电极反应式为4OH-+4e-═O2↑+2H2O,这样做的主要缺点是不能有效利用Pb2+.
(4)用铅蓄电池产生的电量来电解2000mL饱和CuSO4溶液(pH=5)(惰性电极),电解一段时间后测得溶液的pH=1,则铅蓄电池的阳极材料质量变化是6.4g,
(5)电解法制取PbO2,我们可以选择燃料电池做电能.乙醇碱性燃料电池工作时负极的电极反应式为C2H5OH-12e-+16OH-═2CO32-+11H2O,制取478g PbO2时理论上需要乙醇15.3g.
分析 (1)PbO2与浓盐酸共热生成黄绿色气体,说明二者反应生成氯气,同时生成氯化铅和水;
(2)根据电池反应式知,负极电极反应:Pb-2e-+SO42-=PbSO4 ,正极电极反应:PbO2+2e-+4H++2SO42-=PbSO4+2H2O,根据转移电子之间的关系式计算;
(3)PbO2可由PbO与次氯酸钠溶液反应制得,据此可知,PbO与ClO-反应得到PbO2,同时生成Cl-;阳极上Pb2+失去电子,得到PbO2,需要水参与反应,同时生成氢离子,阴极上,Cu2+获得电子生成Cu,附着在石墨电极上;若电解液中不加入Cu(NO3)2,阴极上Pb2+获得电子生成Pb,Pb2+生成PbO2的利用率降低;
(4)铅蓄电池碳棒上已经镀有了铜,故阳极反应是铜失去电子生成铜离子,Cu-2e-=Cu2+,溶液中氢离子浓度为0.1mol/L,物质的量为0.2mol,根据电极方程式为H2O-4e-=4H++O2↑,转移0.2mol电子,根据得失电子守恒计算;
(5)乙醇燃料电池负极为乙醇失去电子发生氧化反应,电极方程式为C2H5OH-12e-+16OH-═2CO32-+11H2O,根据转移的电子数计算.
解答 解:(1)PbO2与浓盐酸共热生成黄绿色气体,说明二者反应生成氯气,同时生成氯化铅和水,反应方程式为PbO2+4HCl(浓)=PbCl2+Cl2↑+2H2O,
故答案为:PbO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$PbCl2+Cl2↑+2H2O;
(2)根据反应知,负极电极反应为Pb-2e-+SO42-=PbSO4 ,当外电路通过2mol电子时,根据反应PbO2+2e-+4H++2SO42-=PbSO4+2H2O,消耗硫酸2mol,
故答案为:Pb-2e-+SO42-=PbSO4 ;2;
(3)PbO2可由PbO与次氯酸钠溶液反应制得,据此可知,PbO与ClO-反应得到PbO2,同时生成Cl-,反应离子方程式为:PbO+ClO-=PbO2+Cl-;阳极上Pb2+失去电子,得到PbO2,需要水参与反应,同时生成氢离子,电极反应式为:Pb2++2H2O-2e-=PbO2↓+4H+,阴极上,Cu2+获得电子生成Cu,附着在石墨电极上,即石墨电极底部有红色物质附着;若电解液中不加入Cu(NO3)2,阳极氢氧根离子放电生成氧气,电极方程式为4OH-+4e-═O2↑+2H2O,阴极上Pb2+获得电子生成Pb,Pb2++2e-=Pb↓,Pb2+的利用率降低,不能有效利用Pb2+,
故答案为:PbO2;石墨电极底部有红色物质附着;4OH-+4e-═O2↑+2H2O;不能有效利用Pb2+;
(4)由上述分析,铅蓄电池碳棒上已经镀有了铜,故阳极反应是铜失去电子生成铜离子,Cu-2e-=Cu2+,用铅蓄电池产生的电量来电解2000mL饱和CuSO4溶液(pH=5)(惰性电极),电解一段时间后测得溶液的pH=1,由于原来溶液中的氢离子浓度太小可忽略,电解过程中,溶液中氢离子浓度为0.1mol/L,物质的量为0.2mol,根据电极方程式为H2O-4e-=4H++O2↑,转移0.2mol电子,由反应Cu-2e-=Cu2+,阳极质量变化为6.4g,
故答案为:6.4;
(5)乙醇燃料电池负极为乙醇失去电子发生氧化反应,电极方程式为C2H5OH-12e-+16OH-═2CO32-+11H2O,根据PbSO4+2H2O-2e-=PbO2+SO42-+4H+,制取478gPbO2时转移电子的物质的量为4mol,则消耗乙醇$\frac{1}{3}$mol,质量为15.3g,
故答案为:C2H5OH-12e-+16OH-═2CO32-+11H2O;15.3.
点评 本题考查内容涉及物质的量的有关计算、离子反应、原电池与电解原理等知识点,(3)中电解液中不加入Cu(NO3)2时阴极反应为易错点,掌握离子放电顺序是关键,题目难度中等.

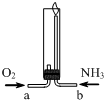
| A. | 气体X的分子式为NO | |
| B. | N2、N4为元素N的两种同素异形体 | |
| C. | 该反应条件下,氨气的还原性小于水 | |
| D. | 两种气体通入的先后顺序是NH3、O2 |
| A. | 苯的一溴代物无同分异构体 | |
| B. | 苯的间二溴代物无同分异构体 | |
| C. | 苯的对二溴代物无同分异构体 | |
| D. | 苯不能使溴水或酸性KMnO4溶液褪色 |
| A. | 己烷与溴的取代反应必须在光照条件下才能进行 | |
| B. | 氯乙烯聚合成聚氯乙烯塑料的本质是加成反应 | |
| C. | 苯与溴的取代反应的催化剂可以是FeBr3,也可以是Fe粉 | |
| D. | 溴乙烷的制取采取加成反应或取代反应的方法都一样 |
| A. | 向NaHSO4溶液中滴加过量Ba(OH)2溶液:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| B. | 用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O═2HCO3-+SO32- | |
| C. | 将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O═SO32-+2HClO | |
| D. | 向碳酸氢钠溶液中加入氢氧化钠:HCO3-+OH-═CO2↑+H2O |
| A. | CH3CH2CH2CH3 | B. | CH3CH(CH3)2 | C. | CH3C(CH3)3 | D. | (CH3)2CHCH2CH3 |
| A. | 当△H为负值时,表示该反应为吸热反应 | |
| B. | 反应热的大小只与反应体系的始态和终态有关 | |
| C. | 反应热的大小与反应物所具有的能量和生成物具有的能量无关 | |
| D. | 热化学方程式2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1,表示2 L氢气和1 L氧气反应放出571.6 kJ的热量 |
 .
.