题目内容
有关容量瓶上的说法错误的是( )
| A、标有温度 |
| B、标有刻度线 |
| C、标有“0”刻度 |
| D、标有容量 |
考点:计量仪器及使用方法
专题:化学实验常用仪器
分析:容量瓶为一种定量仪器,只能用于配制一定体积、浓度的溶液,不能用于溶解、稀释溶质;容量瓶上标有温度、容量及刻度线,没有0刻度线,据此进行解答.
解答:
解:容量瓶是一种用于配制一定物质的量浓度的溶液的定量仪器,容量瓶上标有温度、刻度线及容量,容量瓶上没有具体的小刻度,也没有0刻度线,
所以说法正确的是ABD,错误的是C,
故选C.
所以说法正确的是ABD,错误的是C,
故选C.
点评:本题考查了容量瓶的构造,题目难度不大,注意掌握常见计量仪器的构造及使用方法,明确容量瓶的构造及正确使用方法.

练习册系列答案
相关题目
下列实验操作错误的是( )
| A、称量易潮解、腐蚀性固体药品时,将药品盛放在小烧杯里称量 |
| B、用酒精萃取碘水中的碘,下层液体由分液漏斗下口放出,上层液体由上口倒出 |
| C、不慎将浓碱沾到皮肤上,应立即用大量水冲洗,然后涂上3%的硼酸溶液 |
| D、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
取一定量的饱和氯水与CaCO3粉末混合,观察到氯水的黄绿色褪去,静置后取上层澄清溶液四份,分别进行以下实验:
①一份滴加盐酸,产生大量气泡;
②一份滴加NaOH溶液,出现白色沉淀
③一份用酒精灯加热出现白色沉淀;
④将有色布条浸入第四份溶液,布条立即褪色
根据以上判断下列说法中错误的是( )
①一份滴加盐酸,产生大量气泡;
②一份滴加NaOH溶液,出现白色沉淀
③一份用酒精灯加热出现白色沉淀;
④将有色布条浸入第四份溶液,布条立即褪色
根据以上判断下列说法中错误的是( )
| A、整个实验过程中未涉及氧化还原反应 |
| B、由①、②可知澄清溶液中的含有Ca(HCO3)2 |
| C、②、③中的白色沉淀为CaCO3 |
| D、由④可知澄清溶液中含有HClO |
已知:Fe2O3(s)+C(s)═CO2(g)+2Fe(s)△H=+234.1kJ?mol-1
C(s)+O2(g)=CO2(g)△H=-393.5kJ?mol-1
则2Fe(s)+O2(g)═Fe2O3(s)的△H是( )
C(s)+O2(g)=CO2(g)△H=-393.5kJ?mol-1
则2Fe(s)+O2(g)═Fe2O3(s)的△H是( )
| A、-824.4 kJ?mol-1 |
| B、-627.6kJ?mol-1 |
| C、-744.7kJ?mol-1 |
| D、-168.4kJ?mol-1 |
在 2H2S+SO2═3S↓+2H2O 的反应中,被还原的元素是( )
| A、硫元素 | ||
| B、H2S中的硫元素 | ||
C、
| ||
D、
|
接触法制硫酸和氨氧化法制硝酸分别经过以下主要变化:FeS2
SO2
SO3
H2SO4 NH5
NO
NO2
HNO3
下列说法中正确的是( )
| 1 |
| 2 |
| 3 |
| 4 |
| 5 |
| 6 |
下列说法中正确的是( )
| A、所有变化都是氧化还原反应 |
| B、2、3、4、5四个反应都是化合反应 |
| C、反应2、4、6需要催化剂 |
| D、3是化合反应,6是氧化还原反应 |
微粒
X的质量数为137,中子数为81,则核外电子数为( )
A Z |
| A、54 | B、56 | C、58 | D、137 |
下列递变不正确的是( )
| A、Na、Mg、Al最外层电子数依次增多,其单质的还原性依次减弱 |
| B、P、S、Cl最高正价依次升高,对应气态氢化物稳定性增强 |
| C、C、N、O原子半径依次增大 |
| D、Na、K、Rb氧化物的水化物碱性依次增强 |
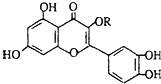 天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P 的叙述错误的是( )
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P 的叙述错误的是( )| A、可以和溴水反应 |
| B、可用有机溶剂萃取 |
| C、分子中有二个苯环 |
| D、1mol维生素P可以和3molNaOH反应 |