题目内容
(探究应用)某学生用下列方法测定CO2的分子的相对质量:先称得充满空气的带塞瓶质量为198.847g,然后用排气法将CO2充满该瓶,又称得其质量为199.190g.最后向该瓶内注水,测知瓶内容积为500mL(以上实验数据均在标准状况下测得).已知标准状况下空气的密度为1.293g?L-1.请你根据他的实验数据列式计算CO2的相对分子质量.分析:相同容积时,气体的物质的量相同,根据瓶的容积可计算容器内气体的物质的量,根据空气的密度可计算容器内空气的质量,进而求出空瓶的质量和瓶内二氧化碳的质量,根据M=
可计算二氧化碳的摩尔质量,进而知道相对分子质量.
| m |
| n |
解答:解法1:容器容积为500mL,则容器中气体的物质的量为:
=
mol,容器中空气的质量为:0.5L×1.293g/L=0.6465g,容器质量为:198.847g-0.6465g=198.2005g,容器中二氧化碳的质量为:199.190g-198.2005=0.9895g,
M=
=44.3296g/mol,相对分子质量和摩尔质量数值相等,故二氧化碳的相对分子质量为44.3296.
答:二氧化碳的相对分子质量为44.3296.
| 0.5L |
| 22.4L/mol |
| 1 |
| 44.8 |
M=
| 0.9895g | ||
|
答:二氧化碳的相对分子质量为44.3296.
点评:本题考查气体相对分子质量的计算,题目难度不大,根据摩尔质量的概念求算,关键要求出空瓶的质量.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
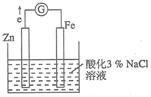 Ⅰ.利用右图装置探究金属的防护措施,实验现象是锌电极不断溶解,铁电极表面有气泡产生。
Ⅰ.利用右图装置探究金属的防护措施,实验现象是锌电极不断溶解,铁电极表面有气泡产生。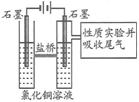 Ⅱ.利用右图装置作电解50mL 0.5mol/L的CuCl2溶液实验。
Ⅱ.利用右图装置作电解50mL 0.5mol/L的CuCl2溶液实验。