题目内容
某温度下,V mL不饱和NaNO3溶液a g,蒸发掉b g水或加入b g NaNO3固体(恢复到原温度)均可使溶液达到饱和,则下列量的计算结果正确的是( )
| A、该温度下NaNO3的溶解度为200 g | ||
B、原不饱和溶液中NaNO3的质量分数为
| ||
C、原不饱和溶液中NaNO3的物质的量浓度为
| ||
D、原不饱和溶液的密度为
|
考点:溶解度、饱和溶液的概念,物质的量浓度的相关计算,溶液中溶质的质量分数及相关计算
专题:
分析:A、依据饱和溶液的组成和溶解度概念分析计算,一定温度下bgNaNO3固体溶于bg水中形成的是饱和溶液;
B、依据饱和溶液的组成和溶质质量分数概念计算分析;
C、不饱和溶液中溶质物质的量和溶液体积减少分析判断;
D、溶液的密度=
.
B、依据饱和溶液的组成和溶质质量分数概念计算分析;
C、不饱和溶液中溶质物质的量和溶液体积减少分析判断;
D、溶液的密度=
| 溶液质量 |
| 溶液体积 |
解答:
解:A、蒸发掉b g水或加入b gNaNO3固体(恢复到原温度)均可使溶液达到饱和,说明一定温度下bgNaNO3固体溶于bg水中形成的是饱和溶液,根据溶解度概念列式计算设溶解度为S,则
=
,
=
,S=100g,故该温度下NaNO3的溶解度为100g,故A错误;
B、设不饱和溶液中溶质为xg,蒸发水bg后为饱和溶液,溶解度为100g,则依据溶解度概念列式计算,
=
,x=
g,所以原不饱和溶液中NaNO3质量分数=
×100%=
×100%=
%,故B错误;
C、设不饱和溶液中溶质为xg,蒸发水bg后为饱和溶液,溶解度为100g,则依据溶解度概念列式计算,原不饱和溶液中NaNO3物质的量浓度=
=
mol/L,故C正确;
D、溶液的密度=
=
=
g/L,故D错误;
故选C.
| 饱和溶液中溶质质量 |
| 饱和溶液中溶剂质量 |
| S |
| 100 |
| bg |
| bg |
| S |
| 100g |
B、设不饱和溶液中溶质为xg,蒸发水bg后为饱和溶液,溶解度为100g,则依据溶解度概念列式计算,
| x |
| a-b |
| 100g |
| 100g+100g |
| a-b |
| 2 |
| 溶质质量 |
| 溶液质量 |
| ||
| a |
| 50(a-b) |
| a |
C、设不饱和溶液中溶质为xg,蒸发水bg后为饱和溶液,溶解度为100g,则依据溶解度概念列式计算,原不饱和溶液中NaNO3物质的量浓度=
| ||||
| V×10-3L |
| 100(a-b) |
| 17V |
D、溶液的密度=
| 溶液质量 |
| 溶液体积 |
| ag |
| V×10-3L |
| 1000a |
| V |
故选C.
点评:本题考查了饱和溶液的组成和溶解度的概念应用,主要是溶解度概念的计算应用、溶质质量分数的计算、物质的量浓度计算.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
一定温度下,将amolPCl5通入一个容积不变的反应器中,达到如下平衡:PCl5(g)?PCl3(g)+Cl2(g),测得平衡混合气体压强为p1,此时再向反应器中通入amolPCl5,在不变的温度下再度达到平衡,测得压强为p2,下列判断正确的是( )
| A、2 p1>p2 |
| B、PCl5的分解率增大 |
| C、2 p1<p2 |
| D、PCl3%(体积含量)增大 |
一氧化碳中毒,是由于一氧化碳跟血液里的血红蛋白结合,使血红蛋白不能很好地跟氧气结合,人因缺少氧气而窒息,甚至死亡.这个反应可表示如下:(血红蛋白-O2)+CO?(血红蛋白-CO)+O2,抢救中毒者采取的措施不正确的是( )
| A、立即打开门窗通风 |
| B、将中毒者转移到空旷的地带 |
| C、立即打开排气扇将CO排出 |
| D、给危重病人及时输氧 |
如图表示汽车尾气净化处理示意图:有关叙述正确的是( )
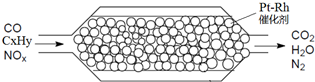

| A、NOX全部被过量CO还原为N2 |
| B、安装有该净化器的汽车可以使用含铅汽油 |
| C、催化剂涂在蜂窝状陶瓷上,可以提高反应速率 |
| D、当产生2.24L氮气时,转移的电子为4xmol |
将标准状况下,将22.4L NH3气体溶于83mL水中,所得溶液密度为0.88g/cm3,则此溶液的物质的量浓度(mol/L)为( )
| A、8.0 mol/L |
| B、8.8 mol/L |
| C、9.0 mol/L |
| D、9.2 mol/L |
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、常温常压下,11.2L氧气所含的原子数为NA |
| B、1.8g的NH4+离子中含有的电子数为10NA |
| C、常温常压下,48g O3含有的氧原子数为3NA |
| D、2.4 g金属镁变为镁离子时失去的电子数为0.1NA |
下列叙述正确的是( )
| A、2.24 L NH3中含有6.02×1022个氮原子 |
| B、100 mL 1 mol/L 的Na2CO3溶液中含有6.02×1022个CO32- |
| C、将4 g NaOH溶于100 g蒸馏水,所得溶液物质的量浓度是0.1 mol/L |
| D、将7.8 g Na2O2放入足量的水中,反应时转移6.02×1022个电子 |