题目内容
7.设阿伏加德罗常数为NA,下列说法正确的是( )| A. | 1.8 g D2O含有的质子数和中子数均为0.1NA | |
| B. | 1 L 0.1 mol•L-1氨水中,所含NH4+的个数为0.1NA | |
| C. | 标准状况下,5.6 L CH3Cl中所含共价键数目为NA | |
| D. | 含0.4 mol溶质的浓硝酸与足量铜片充分反应生成的气体分子数为0.2NA |
分析 A、求出重水的物质的量,然后根据重水中含10个质子和10个中子来分析;
B、一水合氨是弱电解质,不能完全电离;
C、求出一氯甲烷的物质的量,然后根据一氯甲烷中含4条共价键来分析;
D、铜和浓硝酸反应生成二氧化氮,和稀硝酸反应生成NO.
解答 解:A、1.8g重水的物质的量为0.09mol,而重水中含10个质子和10个中子,故0.09mol重水中含质子数和中子数均为0.9NA个,故A错误;
B、一水合氨是弱电解质,不能完全电离,故溶液中铵根离子的个数小于0.1NA个,故B错误;
C、标况下5.6L一氯甲烷的物质的量为0.25mol,而一氯甲烷中含4条共价键,故0.25mol一氯甲烷中含NA条共价键,故C正确;
D、铜和浓硝酸反应生成二氧化氮,和稀硝酸反应生成NO,故0.4mol硝酸和铜反应生成的气体的分子个数无法计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
14.下列物质一定不是天然高分子的是( )
| A. | 橡胶 | B. | 蛋白质 | C. | 腈纶 | D. | 纤维素 |
2.纵观古今,化学与生活皆有着密切联系.下列有关说法错误的是( )
| A. | 氯水中加入稀硫酸,可增强氯水的漂白性 | |
| B. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| C. | 碳酸钾有一定的去污能力,在热水中去污能力会更强 | |
| D. | 《本草纲目》记载的“凡酸坏之酒,皆可蒸烧”的实验方法可用来分离乙酸和乙醇 |
12.松油醇具有紫丁香味,其酯类常用于香精调制.松油醇的结构见图,下列有关松油醇的说法错误的是( )

| A. | 分子式为C10H18O | |
| B. | 分子中有5个碳原子位于同一平面上 | |
| C. | 发生消去反应的有机产物只有一种 | |
| D. | 既能使Br2的CCl4溶液褪色,又能使酸性KMnO4溶液褪色 |
19.下列反应或过程释放能量的是( )
| A. | 化学键形成 | B. | Ba(OH)2•8H2O与NH4Cl反应 | ||
| C. | 生成物能量高于反应物 | D. | 硫磺由固体变为气体 |
16.下列关于物质或离子检验的叙述正确的是( )
| A. | 在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+ | |
| B. | 气体通过无水硫酸铜,粉末变蓝,证明原气体中含有水蒸气 | |
| C. | 向某溶液中加入BaCl2溶液,出现白色沉淀,再加稀硝酸溶液,若沉淀不溶解,则该溶液中肯定有SO42- | |
| D. | 向某溶液中加入Na2CO3溶液,出现白色沉淀,再加稀盐酸,若沉淀消失,则该溶液中肯定有Ca2+ |

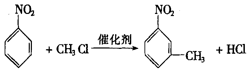 .
.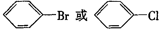 ,②
,② .
.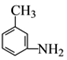 的所有原子不是(填“是”或“不是”)在同一平面上.
的所有原子不是(填“是”或“不是”)在同一平面上.