题目内容
17.原子序数依次增大的四种短周期元素a、b、c、d,a存在a+和a-两种离子,b和d为同一主族元素,b2-和c+的电子层结构相同,下列叙述正确的是( )| A. | 元素的原子半径为d>c>b>a | |
| B. | b,d元素形成的最高价氧化物对应的水化物的酸性b>d | |
| C. | c与其它3种元素均能形成离子化合物 | |
| D. | a、b、c、d四种元素组成的化合物的水溶液可能为酸性、也可能为碱性 |
分析 原子序数依次增大的四种短周期元素a、b、c、d,a存在a+和a-两种离子,则a为H元素;
b和d为同一主族元素,b位于第二周期、d位于第三周期,b2-和c+的电子层结构相同,则b为O元素、c为Na元素、d为S元素,
A.原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小;
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强,但O、F元素除外;
C.活泼金属和活泼非金属元素之间易形成离子键,含有离子键的化合物是离子化合物;
D.a、b、c、d四种元素组成的化合物可能是硫酸氢钠、亚硫酸氢钠.
解答 解:原子序数依次增大的四种短周期元素a、b、c、d,a存在a+和a-两种离子,则a为H元素;
b和d为同一主族元素,b位于第二周期、d位于第三周期,b2-和c+的电子层结构相同,则b为O元素、c为Na元素、d为S元素,
A.原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径c>d>b>a,故A错误;
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强,但O、F元素除外,非金属性b>d,但b没有最高价氧化物的水化物,故B错误;
C.活泼金属和活泼非金属元素之间易形成离子键,含有离子键的化合物是离子化合物,Na与这三种元素分别形成NaH、Na2O、Na2S,这三种钠的化合物都是离子化合物,故C正确;
D.a、b、c、d四种元素组成的化合物可能是硫酸氢钠、亚硫酸氢钠,亚硫酸钠和硫酸氢钠溶液都呈酸性,故D错误;
故选C.
点评 本题考查原子结构和元素周期律,为高频考点,侧重考查学生分析判断能力,明确原子结构、元素周期表结构、物质结构及化合物构成微粒是解本题关键,注意规律中的反常现象,易错选项是BD.

练习册系列答案
相关题目
7.下列说法正确的是( )
| A. | 第IA族元素的金属性比第IIA族元素的金属性强 | |
| B. | 原子最外层只有2个电子的元素一定是第ⅡA元素 | |
| C. | 碱金属的熔点和密度都是随着原子序数的增大而增大 | |
| D. | 如果发现了原子序数为117号元素,它应该属于金属元素 |
8.化学与我们人类生活息息相关,下列说法不正确的是( )
| A. | 合理使用化肥可以提高农作物的产量 | |
| B. | 生活中常使用热的纯碱溶液去除油污 | |
| C. | 明矾具有强氧化性,常用于自来水的杀菌消毒 | |
| D. | 船舶外壳装上锌块可以减缓其腐蚀 |
5.过氧化钙晶体CaO2•8H2O较稳定,呈白色,微溶于水,能溶于酸性溶液.广泛应用于环境杀菌、消毒等领域.过氧化钙晶体含量的测定(假定杂质不发生反应)
准确称取0.3000g产品于锥形瓶中,加入30mL蒸馏水和10mL 2.000mol•L-1 H2SO4,
发生化学反应:CaO2•8H2O+H2SO4═CaSO4+H2O2+8H2O用0.0200mol•L-1KMnO4
标准溶液滴定至终点.H2O2和KMnO4反应的离子方程式为2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O重复上述操作两次.
(1)在滴定过程中,没有选用指示剂是因为高锰酸钾未过量前,溶液是无色的,当溶液变成浅红色.
(2)滴定终点观察到的现象为当滴入最后一滴KMnO4标准溶液后溶液由无色变浅红色,且30s不褪色.
(3)根据表中的数据,计算产品中CaO2•8H2O的质量分数(写出计算过程)
(4)用KMnO4溶液做氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液很容易被空气中或水中某些少量还原性物质还原,生成难溶性物质MnO(OH)2,若用放置了两周的KMnO4标准溶液去测定产品中CaO2•8H2O的质量分数,则测得的值将偏高(填“偏高”或“偏低”)
准确称取0.3000g产品于锥形瓶中,加入30mL蒸馏水和10mL 2.000mol•L-1 H2SO4,
发生化学反应:CaO2•8H2O+H2SO4═CaSO4+H2O2+8H2O用0.0200mol•L-1KMnO4
标准溶液滴定至终点.H2O2和KMnO4反应的离子方程式为2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O重复上述操作两次.
(1)在滴定过程中,没有选用指示剂是因为高锰酸钾未过量前,溶液是无色的,当溶液变成浅红色.
(2)滴定终点观察到的现象为当滴入最后一滴KMnO4标准溶液后溶液由无色变浅红色,且30s不褪色.
(3)根据表中的数据,计算产品中CaO2•8H2O的质量分数(写出计算过程)
| 滴定次数 | 样品的质量/g | KMnO4溶液的体积/mL | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 0.3000 | 1.02 | 26.04 |
| 2 | 0.3000 | 2.00 | 25.02 |
| 3 | 0.3000 | 0.20 | 23.24 |
4.中和热的测定实验中,可能用到下列仪器.其中应使用仪器的正确组合是( )
①托盘天平 ②量筒 ③烧杯 ④温度计 ⑤小试管 ⑥酒精灯.
①托盘天平 ②量筒 ③烧杯 ④温度计 ⑤小试管 ⑥酒精灯.
| A. | ①②⑤ | B. | ②③④ | C. | ②③⑥ | D. | 全部 |
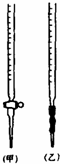 乙二酸俗称草酸,某化学学习小组的同学欲探究测定草酸晶体(H2C2O4•xH2O)中x的值.通过查阅资料该小组同学知道,草酸易溶于水,其水溶液可以用酸性KMnO4溶液进行滴定,反应式为:2MnO4-+5H2C2O4+6H+?2Mn2++10CO2↑+8H2O
乙二酸俗称草酸,某化学学习小组的同学欲探究测定草酸晶体(H2C2O4•xH2O)中x的值.通过查阅资料该小组同学知道,草酸易溶于水,其水溶液可以用酸性KMnO4溶液进行滴定,反应式为:2MnO4-+5H2C2O4+6H+?2Mn2++10CO2↑+8H2O
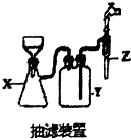
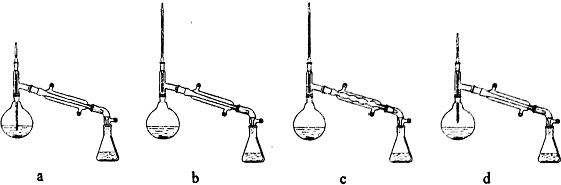
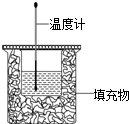 50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程 中放出的热量可计算中和热.回答下列问题:
50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程 中放出的热量可计算中和热.回答下列问题: