题目内容
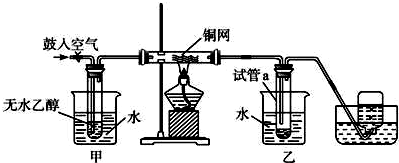
12.实验室将16.8g的铁跟160mL的一定浓度的热浓硝酸反应,测得反应后溶液的体积不变,溶液的c(H+)=1mol/L,生成的NO2和NO混合气体在标准状况下的体积为11.2L.请回答:(1)生成的NO2在标准状况下的体积为4.48L.
(2)原浓硝酸的物质的量浓度为9.75mol/L.
(3)要使上述反应生成的NO2和NO混合气体在NaOH和30%双氧水的混合溶液中全部转化为NaNO3,请计算至少需要30%双氧水51克.
分析 (1)硝酸有剩余,Fe元素被氧化为Fe(NO3)3,计算生成混合气体总物质的量,结合电子注意守恒列方程计算NO2和NO各自物质的量,进而计算NO2的体积;
(2)反应N元素存在于Fe(NO3)3、NO2、NO及剩余的HNO3中,根据N原子守恒计算原浓硝酸中HNO3的物质的量,进而计算原浓硝酸的物质的量浓度;
(3)根据电子转移守恒计算需要过氧化氢的物质的量,进而计算需要30%双氧水的质量.
解答 解:(1)硝酸有剩余,Fe元素被氧化为Fe(NO3)3,反应生成的NO2和NO总物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,消耗Fe的物质的量为$\frac{16.8g}{56g/mol}$=0.3mol,
令NO2、NO的物质的量分别为xmol、ymol,则:
$\left\{\begin{array}{l}{x+y=0.5}\\{x+3y=0.3×3}\end{array}\right.$
解得x=0.3、y=0.2,
NO2的体积=0.2mol×22.4L/mol=4.48L,
故答案为:4.48L;
(2)反应N元素存在于Fe(NO3)3、NO2、NO及剩余的HNO3中,由Fe元素守恒生成Fe(NO3)3为0.3mol,剩余HNO3物质的量为0.16L×1mol/L=0.16mol,
根据N原子守恒,原浓硝酸中HNO3的物质的量=0.3mol×3+0.5mol+0.16mol=1.56mol,则原浓硝酸的物质的量浓度为$\frac{1.56mol}{0.16L}$=9.75mol/L,
故答案为:9.75;
(3)转移电子为0.3mol×3=0.9mol,根据电子转移守恒,需要过氧化氢的物质的量为$\frac{0.9mol}{2}$=0.45mol,需要30%双氧水的质量为$\frac{0.45mol×34g/mol}{30%}$=51g,
故答案为:51.
点评 本题考查混合物计算、氧化还原反应计算,侧重考查学生分析计算能力,注意原子守恒与电子转移守恒的应用.

| A. | 5:2:3 | B. | 5:2:2 | C. | 9:3:1 | D. | 9:3:2 |
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤Si.
| A. | ③④ | B. | ①②③④ | C. | ①③④ | D. | 全部 |
| A. | O.lmol过氧化钠中,阴阳离子总数为0.4 NA | |
| B. | 11.2L氯气通入足量的NaOH充分反应,转移的电子数目为0.5 NA | |
| C. | 17g NH3气体含σ键的数目为3NA | |
| D. | 1L O.lmol/L氨水中,OH-数目为0.1 NA |
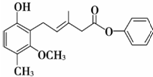
| A. | 该化合物既可以催化加氢,又可以在光照下与Cl2发生取代反应 | |
| B. | 该化合物既可以与溴水反应,又可以使酸性KMnO4溶液褪色 | |
| C. | 该化合物既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2 | |
| D. | 1 mol该化合物最多可以与3mol NaOH反应 |
| A. | 聚乙烯塑料的老化是由于发生了加成反应 | |
| B. | 煤经过干馏等物理变化可以转化为清洁燃料 | |
| C. | 煎炸食物的花生油和牛油都属于酯类,属于高分子化合物 | |
| D. | 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 |
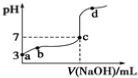
| A. | 由a点推知HA是弱酸 | B. | a、b点的溶液中,水的电离程度:a<b | ||
| C. | c点的溶液中:c(Na+)=c(A-)+c(HA) | D. | d点的溶液中:c(Na+)>c(A-) |
 第四周期过渡元素Mn、Fe、Ti可与C、H、O形成多种化合物.
第四周期过渡元素Mn、Fe、Ti可与C、H、O形成多种化合物.(1)下列叙述正确的是AD.(填字母)
A.HCHO与水分子间能形成氢键
B.HCHO和CO2分子中的中心原子均采用sp2杂化
C.苯分子中含有 6个σ键和1个大π键,苯是非极性分子
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
(2)Mn和Fe的部分电离能数据如下表:
| 元素 | Mn | Fe | |
| 电离能/kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(3)铁原子核外有26种运动状态不同的电子.
(4)根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域,其中Ti属于d区.
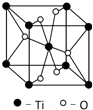
(5)Ti的一种氧化物X,其晶胞结构如图所示,则X的化学式为TiO2.
(6)电镀厂排放的废水中常含有剧毒的CN-离子,可在X的催化下,先用NaClO将CN-氧化成CNO-,再在酸性条件下CNO-继续被 NaClO氧化成N2和CO2.
①H、C、N、O四种元素的电负性由小到大的顺序为H<C<N<O
②与CNO-互为等电子体微粒的化学式为CO2或N2O或SCN-(写出一种即可).
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式N≡C-O-H.