题目内容
某有机物6g与足量Na反应,生成0.05mol H2,该有机物可能是( )
| A、CH3CH2OH |
B、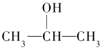 |
| C、CH3OH |
| D、CH3CH2COOH |
考点:有关有机物分子式确定的计算
专题:
分析:根据氢气计算各选项中物质的物质的量,再根据m=nM计算其质量判断,据此判断.
解答:
解:A.乙醇物质的量为0.05mol×2=0.1mol,需要乙醇的质量为0.1mol×46g/mol=4.6g,小于6g,故A错误;
B.2-丙醇物质的量为0.05mol×2=0.1mol,需要2-丙醇醇的质量为0.1mol×60g/mol=6g,故B正确;
C.甲醇物质的量为0.05mol×2=0.1mol,需要甲醇的质量为0.1mol×32g/mol=3.2g,小于6g,故C错误;
D.丙酸物质的量为0.05mol×2=0.1mol,需要丙酸的质量为0.1mol×74g/mol=7.4g,大于6g,故D错误,
故选B.
B.2-丙醇物质的量为0.05mol×2=0.1mol,需要2-丙醇醇的质量为0.1mol×60g/mol=6g,故B正确;
C.甲醇物质的量为0.05mol×2=0.1mol,需要甲醇的质量为0.1mol×32g/mol=3.2g,小于6g,故C错误;
D.丙酸物质的量为0.05mol×2=0.1mol,需要丙酸的质量为0.1mol×74g/mol=7.4g,大于6g,故D错误,
故选B.
点评:本题考查有机物分子确定、化学方程式计算,难度不大,注意利用验证法进行解答.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
下列各组物质中,不管它们以何种比例混合,只要总质量一定,充分燃烧后生成的二氧化碳的量和水的量均不变的是( )
| A、乙炔(C2H2)和甲苯(C7H8) |
| B、乙醇(CH3CH2OH)和丙醇(CH3CH2CH2OH) |
| C、乙醇(CH3CH2OH)和乙醚(C2H5OC2H5) |
| D、甲醛( HCHO)和乙酸(CH3COOH) |
根据陈述的知识,类推得出的结论正确的是( )
| A、镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O |
| B、少量CO2通入Ca(ClO)2溶液生成CaCO3,则少量SO2通入Ca(ClO)2溶液生成CaSO3 |
| C、硝酸银溶液通常保存在棕色的试剂瓶中,是因为硝酸银见光易分解,那么浓硝酸溶液也要保存在棕色试剂瓶中 |
| D、镁比铝活泼,工业上用电解熔融氧化铝制铝,所以工业上也用电解熔融氧化镁制镁 |
某有机物中碳和氢原子个数比为3:4,不能与溴水反应却能使酸性KMnO4溶液褪色.其蒸气密度是相同状况下甲烷密度的7.5倍.在铁存在时与溴反应,能生成两种一溴代物.该有机物可能是( )
| A、CH≡C-CH3 |
B、 |
| C、CH2=CHCH3 |
D、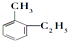 |
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述中正确的是( )
| A、原子半径:A>B>D>C |
| B、原子序数:d>c>b>a |
| C、离子半径:C>D>B>A |
| D、元素的第一电离能:A>B>D>C |
 溴乙烷是一种重要的有机化工原料,其沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸反应.
溴乙烷是一种重要的有机化工原料,其沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸反应.


 某氮肥NH4HCO3中混有少量(NH4)2CO3,现采用下列方案测定该氮肥中(NH4)2CO3的质量分数:称取5.7g上述样品与2.0mol?L-1的NaOH溶液混合,完全溶解后,低温加热使其充分反应(该温度下铵盐不分解),并使生成的氨气全部被硫酸吸收,测得氨气的质量与所用NaOH溶液体积的关系如图所示.
某氮肥NH4HCO3中混有少量(NH4)2CO3,现采用下列方案测定该氮肥中(NH4)2CO3的质量分数:称取5.7g上述样品与2.0mol?L-1的NaOH溶液混合,完全溶解后,低温加热使其充分反应(该温度下铵盐不分解),并使生成的氨气全部被硫酸吸收,测得氨气的质量与所用NaOH溶液体积的关系如图所示.