题目内容
最近上市的苹果NeW采用了新型锂离子电池,该电池以Li2FeSiO4、嵌有Li的石墨为电极,含Li+的导电固体为电解质,充、放电的总反应式可表示为Li2FeSiO4
Li+LiFeSiO4,下列说法中不正确的是( )
| 充电 |
| 放电 |
| A、放电时,电池是将化学能转化为电能 |
| B、放电时,正极反应式:LiFeSiO4+Li++e-═Li2SiO4 |
| C、充电时,毎生成1molLiFeSiO4转移2mol电子 |
| D、充电时,Li+向阴极移动 |
考点:化学电源新型电池,原电池和电解池的工作原理
专题:电化学专题
分析:新型锂离子电池是一种二次电池,放电时,电池是将化学能转化为电能,负极为Li,LiFeSiO4为正极,充电时为电解池,电极反应为原电池中反应的逆过程,充电时,阳离子向阴极移动,阴离子向阳极移动,据此分析.
解答:
解:A.放电时,属于原电池,将化学能转化为电能,故A正确;
B.放电时,正极上LiFeSiO4得电子,则正极反应式:LiFeSiO4+Li++e-═Li2FeSiO4,故B正确;
C.充电时阳极上发生的反应为Li2SiO4-e-═LiFeSiO4+Li+,则毎生成1molLiFeSiO4转移1mol电子,故C错误;
D.充电时,阳离子向阴极移动,则Li+向阴极移动,故D正确.
故选C.
B.放电时,正极上LiFeSiO4得电子,则正极反应式:LiFeSiO4+Li++e-═Li2FeSiO4,故B正确;
C.充电时阳极上发生的反应为Li2SiO4-e-═LiFeSiO4+Li+,则毎生成1molLiFeSiO4转移1mol电子,故C错误;
D.充电时,阳离子向阴极移动,则Li+向阴极移动,故D正确.
故选C.
点评:本题考查原电池的组成和工作原理,题目难度不大,注意把握正负极和阴阳极的判断及电极方程式的书写方法,注意离子的定向移动判断.

练习册系列答案
相关题目
在无色溶液中,下列离子能大量共存的是( )
| A、Na+、NH4+、NO3-、MnO4- |
| B、K +、SO42-、OH-、CO32- |
| C、K +、Fe3+、Cl-、Br- |
| D、Ba2+、Na+、OH-、CO32- |
以下现象不涉及电化学原理的是( )
| A、黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| B、纯铝制品在空气中表面逐渐失去金属光泽 |
| C、锌与稀硫酸反应时,往溶液中滴入几滴CuSO4溶液可以使反应变快 |
| D、与电源的负极相连的金属不易生锈 |
下列说法错误的是( )
| A、化学键的断裂和形成是化学反应中能量变化的主要原因 |
| B、放热反应和吸热反应决定于反应物的总能量与生成物的总能量的相对大小 |
| C、化学反应中能量变化,通常主要表现为热量的变化------放热或者吸热 |
| D、凡经加热而发生的化学反应都是吸热反应 |
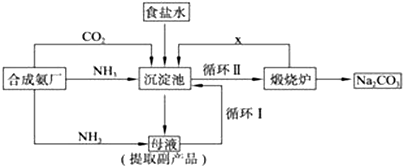
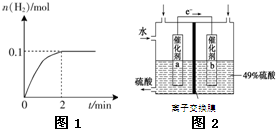 氢能被视为未来的理想清洁能源,科学家预测“氢能”将是21世纪最理想的新能源.目前分解水制氢气的工业制法之一是“硫-碘循环”,主要涉及下列反应:
氢能被视为未来的理想清洁能源,科学家预测“氢能”将是21世纪最理想的新能源.目前分解水制氢气的工业制法之一是“硫-碘循环”,主要涉及下列反应: 研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题.
研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题.