题目内容
15.1mol烷烃,完全燃烧时需要5mol O2,则该烃的C、H原子个数和为( )| A. | 8 | B. | 9 | C. | 11 | D. | 14 |
分析 烷烃通式CnH2n+2,完全燃烧消耗氧气为n+$\frac{2n+2}{4}$,以此计算.
解答 解:1mol烷烃,完全燃烧时需要5mol O2,设烷烃为CnH2n+2,则1mol×(n+$\frac{2n+2}{4}$)=5mol,解得n=3,即C原子个数为3,H原子个数为2×3+2=8,该烃的C、H原子个数和,3+8=11,
故选C.
点评 本题考查有机物燃烧反应的计算,为高频考点,把握有机物完全燃烧消耗氧气的规律为解答的关键,侧重分析与计算能力的考查,注意通式法应用,题目难度不大.

练习册系列答案
相关题目
7.下列叙述中正确的是( )
| A. | 1mol任何气体都含有相同的原子数 | |
| B. | 1molO2中含有6.02×1023个氧分子 | |
| C. | 1molH2中含有1mol氢原子和2mol电子 | |
| D. | 1molH2SO4中含有6NA个原子 |
5.反应4NH3(g)+5O2(g)═4NO(g)+6H2O(g)在10L的密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(x)(反应物的消耗速率或产物的生成速率)可表示为( )
| A. | v(NH3)=0.010mol/(L•s) | B. | v(O2)=0.0010mol/(L•s) | ||
| C. | v(NO)=0.0010mol/(L•s) | D. | v(H2O)=0.045mol/(L•s) |
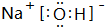 ;
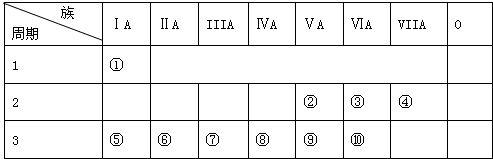
;
 .
. ,该氢化物的水溶液显碱性(填“酸性”、“碱性”或“中性”),该溶液与少量AlCl3溶液反应的离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
,该氢化物的水溶液显碱性(填“酸性”、“碱性”或“中性”),该溶液与少量AlCl3溶液反应的离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+.