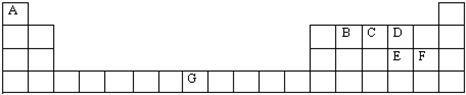
题目内容
(1)相同质量的SO2、SO3的物质的量之比为 ;氧原子的个数之比为 .
(2)19g某二价金属氯化物(ACl2)中含有0.4mol Cl-,则ACl2的摩尔质量是 ;A的相对原子质量是 ;ACl2的化学式是 .
(2)19g某二价金属氯化物(ACl2)中含有0.4mol Cl-,则ACl2的摩尔质量是
考点:物质的量的相关计算
专题:计算题
分析:(1)根据n=
可知,质量相等的SO2、SO3的物质的量之比与其摩尔质量成反比,再结合每个分子含有氧原子数目计算二者含有氧原子数目之比;
(2)计算ACl2的物质的量,再根据M=
计算ACl2的摩尔质量,进而计算A的相对分子质量,确定A为何种元素,书写ACl2的化学式.
| m |
| M |
(2)计算ACl2的物质的量,再根据M=
| m |
| n |
解答:
解:(1)根据n=
可知,质量相等的SO2、SO3的物质的量之比=80g/mol:64g/mol=5:4,含有氧原子数目之比=5×2:4×3=5:6,故答案为:5:4;5:6;
(2)19g某二价金属氯化物(ACl2)中含有0.4mol Cl-,ACl2的物质的量=
=0.2mol,则ACl2的摩尔质量是
=95g/mol,A的相对原子质量是=95-35.5×2=24,故A为Mg元素,ACl2的化学式是MgCl2,
故答案为:95g/mol;24;MgCl2.
| m |
| M |
(2)19g某二价金属氯化物(ACl2)中含有0.4mol Cl-,ACl2的物质的量=
| 0.4mol |
| 2 |
| 19g |
| 0.2mol |
故答案为:95g/mol;24;MgCl2.
点评:本题考查物质的量有关计算,比较基础,注意对基础知识的理解掌握.

练习册系列答案
相关题目
下列有关物质性质的应用错误的是( )
| A、H2O2溶液有氧化性,可用于杀菌消毒 |
| B、氯化镁是一种电解质,可用于电解法制镁 |
| C、液氨汽化时要吸收大量的热,可用作制冷剂 |
| D、Na2SO4能使蛋白质发生变性,可用于提纯蛋白质 |
可逆反应2SO2(g)+O2(g)
2SO3(g)正在逆向进行时,正反应速率和逆反应速率的大小是( )
| A、v正>v逆 |
| B、v正<v逆 |
| C、v正=v逆 |
| D、不能确定 |
下列说法正确的是( )
| A、一氧化碳是不稳定的氧化物,它能继续和氧气反应生成稳定的二氧化碳,故反应一定是吸热反应 |
| B、在101kPa时,1mol碳燃烧所放出的热量为碳的燃烧热 |
| C、物质燃烧都需要氧气 |
| D、物质燃烧放出热量的多少与外界条件有关 |

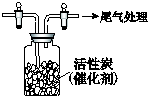 某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2.
某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2.