题目内容
14. 某校化学兴趣小组拟探究碳、硅元素的非金属性的相对强弱,实验装置如图:
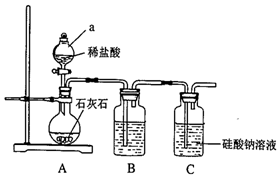
某校化学兴趣小组拟探究碳、硅元素的非金属性的相对强弱,实验装置如图:(1)连接好装置后,实验前必须进行的一步操作是检查装置的气密性.仪器a的名称为分液漏斗.
(2)B装置中盛放的试剂是饱和NaHCO3溶液,C中发生反应的化学方程式为Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓.
(3)该兴趣小组设计此实验依据的原理是元素的最高价氧化物对应的水化物酸性越强,元素的非金属性越强,通过C中有白色胶状沉淀生成(填实验现象),可判断碳的非金属性强于硅的非金属性.请你再列举出一条事实,说明碳的非金{属性强于硅的非金属性:CH4比SiH4稳定或碳单质与氢气化合比硅单质与氢气化合容易.
(4)该小组的一位同学认为,利用此实验装置及药品,也可以证明非金属性Cl>C>Si,你是否同意该同学的观点?不同意(填“同意”或“不同意”).
分析 (1)装置是气体发生装置,连接好后需要检查装置气密性,仪器a为添加溶液的分液漏斗;
(2)装置A是发生装置生成二氧化碳气体中含氯化氢和水蒸气,通过饱和碳酸氢钠溶液吸收氯化氢,二氧化碳通过硅酸钠溶液生成硅酸;
(3)非金属性强弱可以利用元素最高价氧化物对应水化物的酸性比较,判断碳的非金属性强于硅的非金属性,可以利用碳酸和硅酸钠反应生成硅酸证明,也可以利用非金属氢化物的稳定性、与氢气混合难易程度判断非金属性强弱;
(4)证明非金属性Cl>C>Si,需要利用非金属最高价氧化物对应水化物酸性比较或非金属性氢化物稳定性比较.
解答 解:(1)连接好装置后,实验前必须进行的一步操作是检查装置的气密性,仪器a的名称为:分液漏斗,
故答案为:检查装置的气密性;分液漏斗;
(2)装置A是发生装置生成二氧化碳气体中含氯化氢和水蒸气,通过饱和碳酸氢钠溶液吸收氯化氢,二氧化碳通过硅酸钠溶液生成硅酸,反应的化学方程式为:Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓,
故答案为:饱和NaHCO3溶液;Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓;
(3)该兴趣小组设计此实验依据的原理是:元素的最高价氧化物对应的水化物酸性越强,元素的非金属性越强,通过C中有白色胶状沉淀生成,可判断碳的非金属性强于硅的非金属性,说明碳的非金属性强于硅的非金属性的判断是CH4比SiH4稳定或碳单质与氢气化合比硅单质与氢气化合容易,
故答案为:元素的最高价氧化物对应的水化物酸性越强,元素的非金属性越强;C中有白色胶状沉淀生成;CH4比SiH4稳定或碳单质与氢气化合比硅单质与氢气化合容易;
(4)装置A中是碳酸钙和盐酸反应生成二氧化碳,盐酸不是氯元素的最高价含氧酸,利用此实验装置及药品,不可以证明非金属性Cl>C,不同意该同学的观点,
故答案为:不同意.
点评 本题考查性质实验方案的设计、非金属性强弱比较判断,为高频考点,把握气体的制备实验、性质实验、装置的作用及实验技能为解答的关键,侧重分析与设计实验能力的考查,题目难度不大.

 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案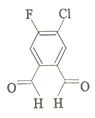 今年春节期间,一个名叫“福(氟)禄(氯)双全(醛)”的物质 (结构简式如图)在化学人的朋友圈中火了起来.该物质属于( )
今年春节期间,一个名叫“福(氟)禄(氯)双全(醛)”的物质 (结构简式如图)在化学人的朋友圈中火了起来.该物质属于( )| A. | 单质 | B. | 无机物 | C. | 有机物 | D. | 氧化物 |
| A. | 其氢氧化物中碱性最强的是NaOH | B. | 单质还原能力最强的是铯 | ||
| C. | 单质熔点最低的是钠 | D. | 原子半径逐渐减少 |
| A. | 硫酸铝铵中Al3+的水解程度比明矾中Al3+的水解程度大 | |
| B. | 该物质的水溶液中Na+、K+、Cl-、S2-都可大量共存 | |
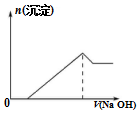
| C. | 向该物质的溶液中滴加同浓度的NaOH溶液的体积与生成沉淀的关系如图所示 | |
| D. | 向该物质的溶液中滴加Ba(OH)2溶液,使SO42-恰好完全沉淀的离子方程式为:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O |
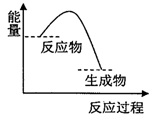
| A. | 该反应过程中,形成新化学键释放的总能量小于断裂旧化学键吸收的总能量 | |
| B. | 因为生成物的总能量低于反应物的总能量,所以该反应不需要加热即可进行 | |
| C. | 该图象可以表示碳酸钙受热分解的能量变化 | |
| D. | 该图象可以表示锌与稀硫酸反应的能量变化 |
| A. | 合金的性能一般优于纯金属 | |
| B. | 碳素钢是目前用量最大的合金,碳素钢在空气中比纯铁耐腐蚀 | |
| C. | 酒精灯加热铝箔至熔化,铝并不滴落,说明铝表面生成一层致密的氧化膜 | |
| D. | 用金属铝与V2O5反应冶炼钒,主要是因为铝的还原能力比钒强 |
| A. | 金属钠着火燃烧时用砂子灭火 | |
| B. | 氯水保存在无色透明的试剂瓶中 | |
| C. | 漂白粉保存在烧杯中 | |
| D. | 大量氯气泄漏时用氢氧化钠溶液浸湿的软布蒙面并迅速离开现场 |
| A. | 用CO2合成聚碳酸酯可降解塑料,可实现“碳”的循环利用 | |
| B. | 油脂都不能使溴的四氯化碳溶液褪色 | |
| C. | 液化石油气和天然气的主要成分都是烃 | |
| D. | 煤是由有机物和少量无机物组成的复杂混合物 |
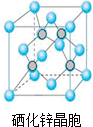 (1)基态硒原子的价层电子排布式为4s24p4.
(1)基态硒原子的价层电子排布式为4s24p4.