题目内容
下列离子或分子能够在指定的分散系中大量共存的是( )
| A、c(H+)=10-13mol/L的溶液中:NO3-、SO42-、K+、Na+ |
| B、澄清石灰水中:Na+、K+、CH3COO -、HCO3- |
| C、铁与稀硫酸反应后的溶液中:[Fe(CN)6]3-、NH4+、Cl-、NO3- |
| D、空气中:SO2、NO、N2、NH3 |
考点:离子共存问题
专题:离子反应专题
分析:A.c(H+)=10-13mol/L<10-7mol/L,抑制水电离,则溶液呈酸性或碱性,离子之间不反应,且和氢离子或氢氧根离子不反应的能大量共存;
B.澄清石灰水溶液呈碱性,溶液中不能大量存在酸式酸根离子;
C.Fe2+、[Fe(CN)6]3-结合生成沉淀;
D.NO不稳定,易被空气氧化.
B.澄清石灰水溶液呈碱性,溶液中不能大量存在酸式酸根离子;
C.Fe2+、[Fe(CN)6]3-结合生成沉淀;
D.NO不稳定,易被空气氧化.
解答:
解:A.c(H+)=10-13mol/L<10-7mol/L,抑制水电离,则溶液呈酸性或碱性,这几种离子之间不反应,能大量共存,故A正确;
B.澄清石灰水溶液呈碱性,OH-、HCO3-和钙离子反应生成碳酸钙沉淀和水,所以不能大量共存,故B错误;
C.铁和稀硫酸反应生成硫酸亚铁,Fe2+、[Fe(CN)6]3-结合生成沉淀,则不能共存,故C错误;
D.NO不稳定,易被空气氧化生成二氧化氮,所以不能存在,故D错误;
故选A.
B.澄清石灰水溶液呈碱性,OH-、HCO3-和钙离子反应生成碳酸钙沉淀和水,所以不能大量共存,故B错误;
C.铁和稀硫酸反应生成硫酸亚铁,Fe2+、[Fe(CN)6]3-结合生成沉淀,则不能共存,故C错误;
D.NO不稳定,易被空气氧化生成二氧化氮,所以不能存在,故D错误;
故选A.
点评:本题考查离子共存,为高考高频点,明确离子性质及离子共存条件是解本题关键,涉及复分解反应、氧化还原反应,易错选项是C,注意Fe2+、[Fe(CN)6]3-的反应.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
下列变化中,能表明硝酸具有氧化性的是( )
| A、石蕊试剂变红色 |
| B、能跟Ag反应生成AgNO3 |
| C、碳酸钙反应 |
| D、能和FeO反应生成Fe(NO3)3 |
下列所示装置中的实验能达到目的是( )
A、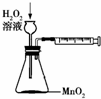 用以定量测定化学反应速率 |
B、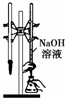 为用已知浓度的氢氧化钠溶液测定未知浓度盐酸的实验 |
C、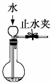 可以检查装置的气密性 |
D、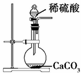 为实验室制取少量CO2的发生装置 |
将2.3g钠放入100g水中,生成溶液中溶质的质量分数是( )
| A、等于2.3% | B、小于4% |
| C、等于4% | D、大于4% |
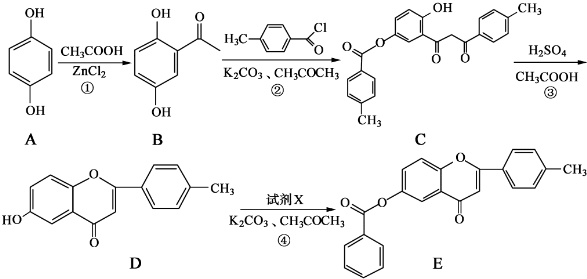

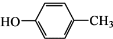 和CH3COOH为原料制备
和CH3COOH为原料制备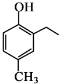 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: 周期表前四周期的元素a、b、c、d、e,原子序数依次增大.a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子.回答下列问题:
周期表前四周期的元素a、b、c、d、e,原子序数依次增大.a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子.回答下列问题: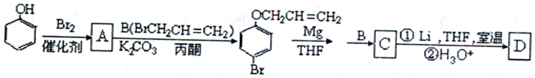
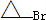 是化合物B的一种同分异构体,用核磁共振氢谱可以证明该化合物中有
是化合物B的一种同分异构体,用核磁共振氢谱可以证明该化合物中有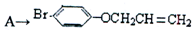 的有机反应类型
的有机反应类型