题目内容
13.银锌电池广泛用作各种电子仪器的电源,其电极分别为Ag2O和Zn,电解质溶液为KOH溶液,总反应为Ag2O+Zn+H2O═2Ag+Zn(OH)2,下列说法中不正确的是( )| A. | 原电池放电时,负极上发生反应的物质是Zn | |
| B. | 负极发生的反应是Zn+2OH--2e-═Zn(OH)2 | |
| C. | 工作时,负极区溶液碱性减弱,正极区溶液碱性增强 | |
| D. | 溶液中OH-向正极移动,K+、H+向负极移动 |
分析 根据电池反应式知,Zn失电子发生氧化反应而作负极,氧化银作正极,负极发生反应Zn+2OH--2e-=ZnO+H2O,溶液pH值减小,正极上发生反应:Ag2O+H2O+2e-═2Ag+2OH-,溶液pH增大,放电时,电解质溶液中阴离子向负极移动、阳离子向正极移动,以此解答该题.
解答 解:A.根据电池反应式知,放电时Zn元素化合价由0价变为+2价,所以负极上Zn失电子发生氧化反应,故A正确;
B.负极上锌失电子发生氧化反应,电极反应式为Zn+2OH--2e-═Zn(OH)2,故B正确;
C.负极发生反应Zn+2OH--2e-=ZnO+H2O,氢氧根离子参加反应导致氢氧根离子浓度降低,则负极区域pH减小;正极反应式为Ag2O+H2O+2e-═2Ag+2OH-,溶液pH增大,故C正确;
D.放电时,电解质溶液中OH-向负极移动,K+、H+向正极移动,故D错误;
故选D.
点评 本题考查化学电源新型电池,为高频考点,明确各个电极上发生的反应是解本题关键,难点是电极反应式的书写,要结合电解质溶液酸碱性书写,易错选项是D,题目难度不大.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
1.工业上粗硅的生产原理为2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,下列说法正确的是( )
| A. | SiO2是氧化剂 | B. | SiO2发生氧化反应 | ||
| C. | C表现出氧化性 | D. | C被还原 |
18.关于氨的下列叙述中,正确的是( )
| A. | 氨具有还原性,可以被氧化为NO | |
| B. | 氨因为有刺激性气味,因此不用来作制冷剂 | |
| C. | 氨极易溶于水,因此氨水比较稳定(不容易分解) | |
| D. | 氨溶于水显弱碱性,因此可使石蕊试液变为红色 |
3.某碱金属1.15g与足量水反应,得到标准状况下0.56L氢气,则该金属是( )
| A. | Li | B. | Na | C. | K | D. | Rb |
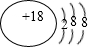 、
、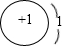 .
.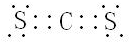 (用元素符号表示),D原子的基态原子核外电子排布式为1s22s22p63s23p4;
(用元素符号表示),D原子的基态原子核外电子排布式为1s22s22p63s23p4;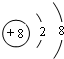 .
.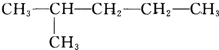 ⑥
⑥