题目内容
11.现有三组混合液:①乙酸乙酯和乙酸钠溶液 ②乙醇和丁醇 ③溴化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )| A. | 分液 蒸馏 萃取 | B. | 萃取 蒸馏 分液 | ||
| C. | 分液 萃取 蒸馏 | D. | 蒸馏 萃取 分液 |
分析 根据题中物质的性质的异同,从溶解性、沸点的角度选择分离方法.
解答 解:①乙酸乙酯和乙酸钠溶液互不相溶,可用分液的方法分离;
②乙醇和丁醇互溶,但沸点不同,可用蒸馏的方法分离;
③溴与溴化钠溶液,可加入苯或四氯化碳,用萃取的方法分离,
故选A.
点评 本题考查物质的分离和提纯,为高考常见题型,侧重于学生的分析能力和实验能力的考查,难度不大,注意把握物质的性质的异同.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
12.醋酸是一种常见的弱酸,为了证明醋酸是弱电解质,某同学开展了题为“醋酸是弱电解质的实验探究”的探究活动.该同学设计了如下方案,其中错误的是( )
| A. | 先配制一定量的0.10 mol/L CH3COOH溶液,然后测溶液的pH,若pH大于1,则可证明醋酸为弱电解质 | |
| B. | 取等体积、等pH的CH3COOH溶液和盐酸分别与足量锌反应,若测得反应过程中醋酸产生H2较慢且最终产生H2较多,则醋酸为弱酸 | |
| C. | 先配制一定量0.01 mol/L的CH3COOH和0.10 mol/L的CH3COOH,分别用pH计测它们的pH,若两者的pH相差小于1个单位,则可证明醋酸是弱电解质 | |
| D. | 配制一定量的CH3COONa溶液,测其pH,若常温下pH大于7,则可证明醋酸是弱电解质 |
2.下列关于金属元素性质的叙述正确的是( )
| A. | 金属元素的原子只有还原性,离子只有氧化性 | |
| B. | 金属元素在化合物中一定县正化合价 | |
| C. | 金属元素在不同化合物中化合价一定不同 | |
| D. | 金属元素的单质在常温下都是固体 |
19.下列是四种烃的碳骨架,以下关于四种烃的说法不正确的是( )
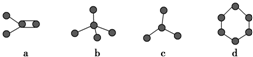

| A. | a能使高锰酸钾酸性溶液褪色 | B. | b的分子式为C5H12 | ||
| C. | b和c互为同系物 | D. | d为平面形分子,属于烷烃 |
6.下列分子式可以表示3种沸点不同的物质的是( )
| A. | C5H12 | B. | C4H10 | C. | C3H8 | D. | C2H6 |
16.核能是人类最具希望的未来能源,安全、合理地开发利用核能日益受到人们的关注.${\;}_{92}^{235}$U是核反应堆的重要原料,下列说法中正确的是( )
| A. | ${\;}_{92}^{235}$U的中子数为235 | |
| B. | ${\;}_{92}^{235}$U和${\;}_{92}^{238}$U是两种核素,它们互称为同素异形体 | |
| C. | 核反应属于化学变化 | |
| D. | 合理利用核能符合“低碳经济”要求 |
3.下列关于铝及其化合物的说法中不正确的是( )
| A. | 铝既可以用于食品包装,也可以用于建筑材料 | |
| B. | 氧化铝既可以用来冶炼铝,也可用作耐火材料 | |
| C. | 氢氧化铝既可以用于治疗胃酸过多,也可用来制备一些铝盐 | |
| D. | 明矾既能用来净水,也可用作消毒剂 |
20.25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合:c(Na+)=c(Cl-)>cCH3COO-)>c(OH-) | |
| B. | 0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| C. | 0.1mol/LNa2CO3与0.1mol/L NaHCO3溶液等体积混合:3(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)] | |
| D. | 0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) |
1.氢氧燃料电池已用于航天飞机,以30%KOH溶液为电解质溶液.电极反应如下:2H2+4OH--4e-=4H2O,O2+2H2O+4e-=4OH-.据此作出判断,下列说法中不正确的是( )
| A. | O2在正极发生还原反应 | B. | 供电时的总反应为2H2+O2═2H2O | ||
| C. | 燃料电池的能量转化率可达100% | D. | 氢氧燃料电池属于环境友好电池 |