题目内容
5.有四种化合物:①NaHCO3、②Al(OH)3、③(NH4)2S、④H2NCH2COOH,跟盐酸和氢氧化钠溶液都能反应的是( )| A. | 只有②④ | B. | 只有①② | C. | 只有①②③ | D. | ①②③④ |
分析 既能与盐酸反应又能与氢氧化钠溶液反应的物质有:两性化合物(如Al2O3、Al(OH)3等)、弱酸的铵盐(如(NH4)2CO3、(NH4)2S等)、弱酸的酸式盐(NaHCO3、NaHS等)、单质(如Al)、氨基酸等,据此解答.
解答 解:①NaHCO3是弱酸的酸式盐,与盐酸反应生成氯化钠、二氧化碳和水,与氢氧化钠溶液反应生成碳酸钠和水,故①正确;
②Al(OH)3 是两性氢氧化物,与盐酸反应生成绿化铝和水,与氢氧化钠溶液反应生成偏铝酸钠和水,故②正确;
③(NH4)2S是弱酸弱碱盐,与盐酸反应生成氯化铵和硫化氢气体,与氢氧化钠反应生成硫化钠、氨气和水,故③正确;
④H2N-CH2-COOH是两性物质,与盐酸、氢氧化钠反应产物都是盐和水,故④正确;
故选D.
点评 本题考查了元素化合物的性质,明确物质的性质是解本题的关键,注意对既能与盐酸反应又能与氢氧化钠溶液反应的物质的积累,题目难度不大.

练习册系列答案
相关题目
15.一定条件下,下列各组物质中,Y既能与X反应又能与Z反应的有几组( )
| 序号 | X | Y | Z |
| ① | NaHSO4溶液 | Al(OH)3 | 稀硫酸 |
| ② | CaCl2溶液 | SO2 | CaSO3 |
| ③ | HF溶液 | Si | Ba(OH)2 |
| ④ | Fe Cl3溶液 | Fe | 浓硝酸 |
| A. | 1组 | B. | 2组 | C. | 3组 | D. | 4组 |
16.下列有关维生素C的说法中,正确的是( )
| A. | 如果人体缺少维生素C,易患夜盲症、干眼症等眼疾 | |
| B. | 维生素C属于脂溶性维生素,主要存在于新鲜水果和蔬菜中 | |
| C. | 维生素C具有较强的还原性,能使酸性高锰酸钾溶液褪色 | |
| D. | 富含维生素C的食物应在高温下烹调,才能充分提高维生素C的功能 |
20.下列气态氢化物中,按稳定性由强到弱的顺序排列的是( )
| A. | HI、HBr、HCl、HF | B. | HCl、H2S、PH3、SiH4 | ||
| C. | H2O、H2S、HCl、HBr | D. | H2O、HF、NH3、CH4 |
10.用如图装置完成相关实验,不合理的是( )
| A. | 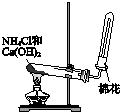 制备并收集氨气 | B. |  制备氯气 | ||
| C. | 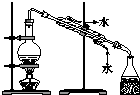 蒸馏海水得到淡水 | D. | 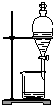 分离Na2CO3溶液与CH3COOC2H5 |
17.关于如图各实验装置的叙述中,不正确的是( )
| A. | 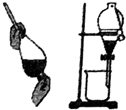 可用于分离苯和水的混合物 | |
| B. | 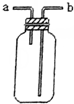 可用于收集H2、NH3、CO2、Cl2、HCl等气体 | |
| C. | 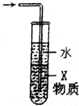 X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 | |
| D. | 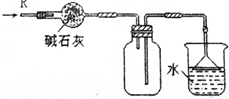 可用于干燥、收集氯化氢,并吸收多余的氯化氢 |
14.表为元素周期表的一部分.
回答下列问题
(1)Z元素在周期表中的位置为第三周期,第ⅤⅡA族.
(2)表中元素的原子半径最大的是(填元素符号)Si.
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是ac;
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)X与Z两元素的单质反应生成8.5gX的最高价化合物,恢复至室温,放热34.35kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出该反应的热化学方程式Si(s)+2Cl2(g)=SiCl4(l)△H=-687kJ/mol.
(5)碳与铝形成的1mol化合物Q与水反应,生成4molAl(OH)3和3mol化合物L(仅含碳、氢两种元素),则L的电子式为 .
.
(6)H2Y2是实验室中的常用试剂,其结构中存在的共价键有和,在制备过程中要防止Fe3+的混入,理由是铁离子对过氧化氢分解起到催化剂作用,.
| 碳 | 氮 | Y | |
| X | 硫 | Z |
(1)Z元素在周期表中的位置为第三周期,第ⅤⅡA族.
(2)表中元素的原子半径最大的是(填元素符号)Si.
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是ac;
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)X与Z两元素的单质反应生成8.5gX的最高价化合物,恢复至室温,放热34.35kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出该反应的热化学方程式Si(s)+2Cl2(g)=SiCl4(l)△H=-687kJ/mol.
(5)碳与铝形成的1mol化合物Q与水反应,生成4molAl(OH)3和3mol化合物L(仅含碳、氢两种元素),则L的电子式为
 .
.(6)H2Y2是实验室中的常用试剂,其结构中存在的共价键有和,在制备过程中要防止Fe3+的混入,理由是铁离子对过氧化氢分解起到催化剂作用,.