题目内容
在相同温度下,下列两个反应放出的热量分别用Q1和Q2表示:则下列关系正确的是( )H2(g)+
O2(g)=H2O(g)△H=-Q1kJ/mol2H2(g)+O2(g)=2H2O(l)△H=-Q2kJ/mol.
| 1 |
| 2 |
| A、Q1=Q2 | ||
B、
| ||
C、Q1<
| ||
D、Q1=
|
考点:反应热和焓变
专题:化学反应中的能量变化
分析:H2O(g)=H2O(l)△H<0,利用盖斯定律进行判断.
解答:
解:已知H2O(g)=H2O(l)△H<0,
则有H2O(g)=H2O(l)△H=(-Q2kJ/mol)-2(-Q1kJ/mol)<0,
可得Q1<
Q2,
故选C.
则有H2O(g)=H2O(l)△H=(-Q2kJ/mol)-2(-Q1kJ/mol)<0,
可得Q1<
| 1 |
| 2 |
故选C.
点评:本题考查反应的比较问题,题目难度不大,注意气态水生成液态水为放热过程,利用盖斯定律比较反应热的大小.

练习册系列答案
相关题目
将镁粉和碳酸镁的混和物置于氧气中灼烧,直至质量不再改变为止,经测定,灼烧后所得的固体质量与原混和物的质量相同,则原混和物中镁粉和碳酸镁的质量比为( )
| A、4:7 | B、10:7 |
| C、14:11 | D、11:14 |
Cl2是纺织工业常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”.”.S2O32-和Cl2反应的产物之一为SO42-下列说法不正确的是( )
| A、该反应中还原剂是S2O32- |
| B、H2O参与该反应,且作氧化剂 |
| C、根据该反应可判断氧化性:Cl2>SO42- |
| D、上述反应中,每生成1 molSO42-,可脱去2 mol Cl2 |
某饮用水的理化指标:钙≥4.0mg/L、钾≥0.35mg/L、钠≥0.8mg/L、镁≥0.5mg/L,以上钙、钾、钠、镁指的是( )
| A、分子 | B、氧化物 | C、元素 | D、单质 |
物质的量之比为1:3的锌与稀硝酸混合,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,下列说法正确的是( )
| A、在此反应中硝酸只体现强氧化性 |
| B、向反应后的溶液中再加入金属铁,不再发生化学反应 |
| C、该反应中被还原的硝酸与未被还原的硝酸之比为1:4 |
| D、该反应中被还原的硝酸与未被还原的硝酸之比为1:5 |
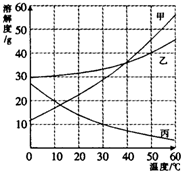 甲、乙、丙三种物质的溶解度曲线如右图所示.据图回答:
甲、乙、丙三种物质的溶解度曲线如右图所示.据图回答: