题目内容
16.常温下,下列有关电解成溶液的说法正确的是( )| A. | pH=2的H2SO4与pH=12的NaOH等体积混合,所得溶液呈酸性 | |
| B. | 0.1mol/L的CH3COOH溶液在加水稀释过程中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$减小 | |
| C. | pH=5的NaHSO4溶液中水的电离程度小于纯水的电离程度 | |
| D. | 0.1mol/L的NaHCO3溶液中:c(OH-)═(H+)+2c(H2CO3)+c(HCO3-) |
分析 A.常温下Kw=10-14,pH=2的H2SO4与pH=12的NaOH等体积混合,c(OH-)═(H+);
B.加水稀释时Ka、Kw不变,$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$=$\frac{c(C{H}_{3}CO{O}^{-})c({H}^{+})}{c(C{H}_{3}COOH)•Kw}$=$\frac{Ka}{Kw}$;
C.NaHSO4溶液电离显酸性,抑制水的电离;
D.电荷守恒式为c(OH-)+c(HCO3-)+2c(CO32-)═c(H+)+c(Na+),物料守恒式为c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-).
解答 解:A.常温下Kw=10-14,pH=2的H2SO4与pH=12的NaOH等体积混合,c(OH-)═(H+),则溶液为中性,故A错误;
B.加水稀释时Ka、Kw不变,$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$=$\frac{c(C{H}_{3}CO{O}^{-})c({H}^{+})}{c(C{H}_{3}COOH)•Kw}$=$\frac{Ka}{Kw}$,则加水稀释过程中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$不变,故B错误;
C.NaHSO4溶液电离显酸性,抑制水的电离,则pH=5的NaHSO4溶液中水的电离程度小于纯水的电离程度,故C正确;
D.电荷守恒式为c(OH-)+c(HCO3-)+2c(CO32-)═c(H+)+c(Na+),物料守恒式为c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-),则c(OH-)═(H+)+c(H2CO3)-c(CO32-),故D错误;
故选C.
点评 本题考查酸碱混合,为高频考点,把握溶液酸碱性、电荷及物料守恒的应用为解答的关键,侧重分析与应用能力的考查,注意选项B为解答的难点,题目难度不大.

| A. | Ge(32号元素)的单晶可以作为光电转换材料用于太阳能电池 | |
| B. | 交警检查司机是否酒后驾车的原理中体现了乙醇的还原性 | |
| C. | 在家用电热水器不锈钢内胆镶嵌镁棒,以防止内胆被腐蚀 | |
| D. | 施用适量石灰乳可降低盐碱地(含较多NaCl、Na2CO3)的碱性 |
| X | Y | Z |
| W |
| A. | Z元素的常见化合价为:-1、-2 | |
| B. | X元素的氢化物的沸点一定比Z的低 | |
| C. | Y、Z、W形成的简单离子中,半径最小的是Z | |
| D. | Z元素的单质能从Na2W溶液中置换出W的单质 |
| A. | 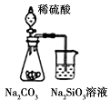 此装置可证明非金属性强弱:S>C>Si | |
| B. | 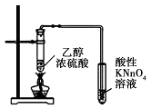 此装置可用于检验有乙烯生成 | |
| C. | 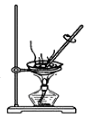 此装置可通过蒸干AlCl3饱和溶液制备AlCl3晶体 | |
| D. | 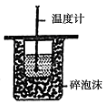 此装置可用来测定中和热 |
| A. | 硅胶可用作食品的抗氧化剂 | |
| B. | 可用热碱水清洗炊具上的油渍 | |
| C. | 铁表面镀锌可增强其抗腐蚀性 | |
| D. | 大量燃烧化石燃料是导致雾霾天气的重要因素之一 |
| 选项 | 操 作 | 现 象 | 结 论 |
| A | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状炭,并放出有剌激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
| B | 向盛有H2O2溶液的试管中加入几滴酸化的硫酸亚铁溶液 | 溶液变成棕黄色,一段时间后,溶液中出现气泡,随后有红褐色沉淀生成 | Fe2+催化H2O2分解产生O2;H2O2分解反应放热,促进Fe3+的水解平衡正向移动 |
| C | 铝片先用砂纸打磨,再加入 到浓硝酸中 | 无明显现象 | 浓硝酸具有强氧化性,常温下,铝被浓硝酸钝化 |
| D | 向等浓度的KC1、KI混合液中逐滴满加AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp (AgI) |
| A. | A | B. | B | C. | C | D. | D |
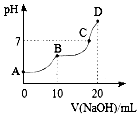 25℃时,向10mL 0.1mol•L-1 H2A溶液中滴加等浓度的NaOH溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列叙述错误的是( )
25℃时,向10mL 0.1mol•L-1 H2A溶液中滴加等浓度的NaOH溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列叙述错误的是( )| A. | C点溶液中含有NaHA和Na2A | |
| B. | NaHA溶液中水的电离程度比Na2A溶液中小 | |
| C. | B点,c (Na+)=2[c (H2A)+c (HA)+c (A2-)] | |
| D. | D点,c (Na+)>c (A2-)>c (OH-)>c (HA-)>c (H+) |
①H2;②CO;③H2和CO的混合气体;④HCOOCH3;⑤CH3CHO;⑥C6H12O6.
| A. | ①②③⑤⑥ | B. | ②③④⑤ | C. | ①②③④⑥ | D. | ①②③④⑤ |
| A. |  | B. |  | ||
| C. |  | D. |  |