题目内容
将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)?xC(g)+2D(g),
经5min后,测得D的浓度为0.5mol?L-1,C的平均反应速率是0.1mol/(L?min),且此时A、B的物质的量浓度之比为3:5.求:
(1)x的值是 .
(2)B的平均反应速率为 .
(3)反应开始前放入容器中A的物质的量为 .
经5min后,测得D的浓度为0.5mol?L-1,C的平均反应速率是0.1mol/(L?min),且此时A、B的物质的量浓度之比为3:5.求:
(1)x的值是
(2)B的平均反应速率为
(3)反应开始前放入容器中A的物质的量为
考点:化学平衡的计算
专题:化学平衡专题
分析:(1)根据同一反应中反应速率之比等于化学计量数之比求出x值;
(2)先求出反应的B的物质的量,再根据平均反应速率公式计算B的平均反应速率;
(3)根据D的浓度求出D的物质的量,结合方程式求出A、B的物质的量.
(2)先求出反应的B的物质的量,再根据平均反应速率公式计算B的平均反应速率;
(3)根据D的浓度求出D的物质的量,结合方程式求出A、B的物质的量.
解答:
解:(1)根据同一反应中反应速率之比等于化学计量数之比,所以v(B):v(C)=0.05 mol/(L.min):0.1mol/(L?min)=1:x,所以x=2.
故答案为:2;
(2)设反应的B的物质的量为n,依据化学平衡三段式列式计算,经5min后,测得D的浓度为0.5mol?L-1,D的物质的量=2L×0.5mol?L-1=1mol;
3A(g)+B(g)?2C(g)+2D(g),
起始量(mol) 1 2
变化量(mol) n 1
n=0.5 mol
根据v(B)=
=0.05 mol/(L.min)
故答案为:0.05 mol/(L.min);
(3)5分钟后,n(D)=CV=0.5mol/L×2L=1mol,设反应开始前放入容器中A、B物质的量为m,
3A(g)+B(g)?2C(g)+2D(g),
反应前 (mol) m m 0 0
5分钟后 ( m-1.5)( m-0.5)1
c(A):c(B)=3:5=( m-1.5):( m-0.5)
m=3 mol
故答案为:3mol.
故答案为:2;
(2)设反应的B的物质的量为n,依据化学平衡三段式列式计算,经5min后,测得D的浓度为0.5mol?L-1,D的物质的量=2L×0.5mol?L-1=1mol;
3A(g)+B(g)?2C(g)+2D(g),
起始量(mol) 1 2
变化量(mol) n 1
n=0.5 mol
根据v(B)=
| ||
| 5min |
故答案为:0.05 mol/(L.min);
(3)5分钟后,n(D)=CV=0.5mol/L×2L=1mol,设反应开始前放入容器中A、B物质的量为m,
3A(g)+B(g)?2C(g)+2D(g),
反应前 (mol) m m 0 0
5分钟后 ( m-1.5)( m-0.5)1
c(A):c(B)=3:5=( m-1.5):( m-0.5)
m=3 mol
故答案为:3mol.
点评:本题考查了化学反应速率与化学计量数的关系,明确同一反应中反应速率之比等于化学计量数之比是解(1)的关键,题目难度中等.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
下列条件的变化对醋酸的电离常数产生影响的是( )
| A、增大醋酸的浓度 |
| B、向溶液中加水 |
| C、增大压强 |
| D、升高温度 |
从下列混合物中分离出其中的一种成分,所采取的分离方法正确的是( )
| A、由于碘在酒精中的溶解度大,可以用酒精把碘水中的碘萃取出来 |
| B、水的沸点为100℃,酒精的沸点为78.5℃,所以用加热蒸馏的方法使含水的酒精变为无水酒精 |
| C、由于沙子和水不相溶,因此可用过滤法分离沙子与水的混合物 |
| D、NaCl的溶解度随温度下降而减小,可以用冷却法从热的含少量的KNO3的NaCl浓溶液中分离得到纯净的NaCl |
在给定的四种溶液中,加入以下各种离子后,各离子能在原溶液中大量共存的有( )
| A、滴加酚酞试液显红色的溶液:Fe2+、NH4+、Cl-、I- |
| B、水电离出来的C (H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ |
| C、在C (H+)=10-13mol/L的溶液:K+、SO42-、Al3+、Cl- |
| D、PH=1的溶液:Cu2+、Na+、Mg2+、NO3- |
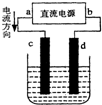 如图是电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是( )
如图是电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是( )| A、a为负极、d为阳极 |
| B、将淀粉KI试纸的玻璃棒靠近d处一段时间会变蓝色 |
| C、电解过程中转移0.2mol电子,d电极质量增加6.4克 |
| D、电解过程中,铜离子向C极移动 |
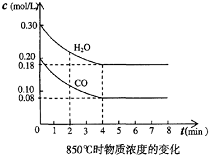 (1)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g);△H<0
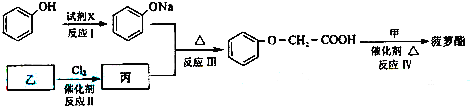
(1)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g);△H<0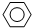 -O-CH2-COOH发生酯化反应的产物.
-O-CH2-COOH发生酯化反应的产物.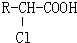 R-ONa
R-ONa