题目内容
燃烧0.1mol两种气态烃的混合物,生成3.58L CO2(标准状况)和3.6g H2O,则混合气体的组成为( )
| A、CH4、C2H6 |
| B、CH4、C2H4 |
| C、C2H4、C2H6 |
| D、C2H4、C3H6 |
考点:有关混合物反应的计算
专题:烃及其衍生物的燃烧规律
分析:0.1mol混合烃完全燃烧生成二氧化碳的物质的量为:n(CO2)=
=0.16mol,水的物质的量为:n(H2O)=
=0.2mol,则混合的平均化学式为C1.6H4,因是混合物,则肯定含有C原子数小于1.6的烃,即一定含有甲烷,因甲烷中含有4个氢原子,则另一种烃也含有4个氢原子,以此解答该题.
| 3.58L |
| 22.4L/mol |
| 3.6g |
| 18g/mol |
解答:
解:0.1mol两种气态烃燃烧生成二氧化碳、水的物质的量为:n(CO2)=
=0.16mol,n(H2O)=
=0.2mol,
则混合的平均化学式为C1.6H4,
由于是混合物,则一定含有C原子数小于1.6的烃,即一定含有甲烷,
因甲烷中含有4个氢原子,则另一种烃也含有4个氢原子,
A.CH4、C2H6:乙烷分子中含有6个H原子,故A错误;
B.CH4、C2H4:二者分子中都含有4个H,平均分子式可以满足C1.6H4,故B正确;
C.C2H4、C2H6:二者平均碳原子数为2,不属于1.6,平均氢原子也不是4,故C错误;
D.C2H4、C3H6:二者平均碳原子数一定大于2,平均氢原子一定大于4,故D错误
故选B.
| 3.58L |
| 22.4L/mol |
| 3.6g |
| 18g/mol |
则混合的平均化学式为C1.6H4,
由于是混合物,则一定含有C原子数小于1.6的烃,即一定含有甲烷,
因甲烷中含有4个氢原子,则另一种烃也含有4个氢原子,
A.CH4、C2H6:乙烷分子中含有6个H原子,故A错误;
B.CH4、C2H4:二者分子中都含有4个H,平均分子式可以满足C1.6H4,故B正确;
C.C2H4、C2H6:二者平均碳原子数为2,不属于1.6,平均氢原子也不是4,故C错误;
D.C2H4、C3H6:二者平均碳原子数一定大于2,平均氢原子一定大于4,故D错误
故选B.
点评:本题考查分子式的确定、混合物计算,题目难度中等,解答关键是利用平均分子组成判断烃的组成,明确常用的计算方法:平均碳法、平均氢法、平均碳氢分子式法、平均式量法.

练习册系列答案
 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,11.2L的二氯甲烷所含的分子数为0.5NA |
| B、28g乙烯所含共用电子对数目为4NA |
| C、现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
| D、1mol甲基的电子数目为7NA |
在铁制品上镀上一定厚度的铜层,以下电镀方案中正确的是( )
| A、铜作阳极,铁制品作阴极,溶液中含Fe2+ |
| B、铜作阴极,铁制品作阳极,溶液中含Cu2+ |
| C、铜作阴极,铁制品作阳极,溶液中含Fe3+ |
| D、铜作阳极,铁制品作阴极,溶液中含Cu2+ |
化学与社会、科学、技术、环境密切相关.下列说法不正确的是( )
| A、预防H7N9流感病毒的措施之一是高温消毒餐具等生活用品 |
| B、《添加剂标准》中儿童膨化食品拟禁含铝添加剂,铝对人体有害 |
| C、绿色化学的核心是应用化学原理对环境污染进行治理 |
| D、明矾、硫酸铁等在水中因水解生成胶体粒子,都可以作净水剂 |
下列装置所示的实验中,能达到实验目的是( )
A、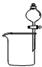 分离碘酒中的碘和酒精 |
B、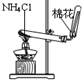 实验室制氧气 |
C、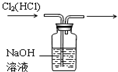 除去Cl2中的HCl |
D、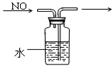 排水集气法收集NO |
0.116g饱和一元醛,进行银镜反应时析出0.432g银.则该醛为( )
| A、丙醛 | B、乙醛 | C、甲醛 | D、苯酚 |
下列反应条件的控制中,不恰当的是( )
| A、为了防止铁生锈,在其表面涂一层防锈油漆 |
| B、为防止火灾,在面粉厂、加油站等场所要严禁烟火 |
| C、为加快KClO3的分解速率,加入MnO2 |
| D、为加快H2O2的分解速率,把反应容器放到冷水中冷却 |