题目内容
6.实验室用已知密度的37%的盐酸配制15%的盐酸,除量筒、烧杯外还需使用下列仪器中的( )| A. | 托盘天平 | B. | 容量瓶 | C. | 玻璃棒 | D. | 胶头滴管 |
分析 实验室用37%的盐酸配置15%的盐酸,需量取浓盐酸的体积和水的体积,且需使用烧杯作为容器稀释,玻璃棒搅拌,据此进行解答.
解答 解:实验室用37%的盐酸配置15%的盐酸,需计算出浓盐酸的体积和水的体积,需用量筒量取,浓盐酸稀释为稀盐酸,需用烧杯作为容器,玻璃棒搅拌加速溶解,所以还需要玻璃杯,
故选C.
点评 本题考查了配制一定质量分数的溶液方法,题目难度不大,明确配制溶液步骤为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及化学实验能力.

练习册系列答案
相关题目
16.下表是元素周期表的一部分,表中的每个字母代表一种短周期元素.
(1)a元素和b元素可以形成最简单的有机物,其化学式为CH4;
(2)e元素位于第三周期第ⅠA族,它的元素符号是Na;
(3)c元素原子的最外层电子数为5;
(4)b、c、d三种元素的非金属性逐渐增强(填“减弱”或“增强”);
(5)f的元素符号为S.
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | a | |||||||
| 2 | b | c | d | |||||
| 3 | e | f | ||||||
(2)e元素位于第三周期第ⅠA族,它的元素符号是Na;
(3)c元素原子的最外层电子数为5;
(4)b、c、d三种元素的非金属性逐渐增强(填“减弱”或“增强”);
(5)f的元素符号为S.
17.工业上真空炼铷的反应方程式为2RbCl2+Mg$\stackrel{熔融}{?}$MgCl2+2Rb↑,对此反应能够进行正确解释的是( )
| A. | 高温下Mg2+得电子的能力比Rb+弱 | |
| B. | MgCl2对热的稳定性比RbCl强 | |
| C. | 在一定条件下,Mg的金属性比Rb强 | |
| D. | 铷的沸点比镁低,及时抽走铷蒸气使平衡向正反应方向移动 |
1.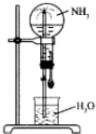 四个等体积的圆底烧瓶分别充满①NH3②HCl③NO2④NO2和O2的混合物进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度大小关系为( )
四个等体积的圆底烧瓶分别充满①NH3②HCl③NO2④NO2和O2的混合物进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度大小关系为( )
 四个等体积的圆底烧瓶分别充满①NH3②HCl③NO2④NO2和O2的混合物进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度大小关系为( )
四个等体积的圆底烧瓶分别充满①NH3②HCl③NO2④NO2和O2的混合物进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度大小关系为( )| A. | ①>②>③>④ | B. | ①=②=③=④ | C. | ①=②=③>④ | D. | ①=②>③>④ |
11.银锌钮扣电池的两个电极分别是由氧化银与少量石墨组成的活性材料和锌汞合金构成,电解质为氢氧化钾溶液,电极反应为 Zn+2OH--2e-═ZnO+H2O;Ag2O+H2O+2e-═2Ag+2OH-;总反应为:Ag2O+Zn═2Ag+ZnO,下列判断正确的是( )
| A. | 锌为正极,Ag2O为负极 | |
| B. | 如果有1mol电子转移,就有32.5g Zn参加反应 | |
| C. | 原电池工作时,正极区PH减小 | |
| D. | 锌为阳极,Ag2O为阴极 |
16.X、Y、Z、W四种主族元素分属于元素周期表的前三周期,原子序数依次增加,它们原子的最外层电子数之和为15,Y2-和Z2+的电子层结构相同.下列说法正确的是( )
| A. | 氢化物的沸点:Y<W | |
| B. | 简单离子的半径:W>Y>Z>X | |
| C. | W的氧化物对应的水化物是一种强酸 | |
| D. | 与Z同族的下一周期元素的单质不能与N2反应 |

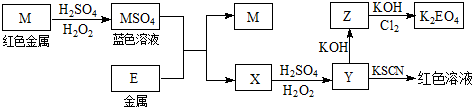


 (R、R′可以是氢原子、烃基或官能团)
(R、R′可以是氢原子、烃基或官能团) .
. .
. .
.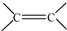 和
和 结构的D的所有同分异构共有7种(不包括顺反异构体),写出其中任意两种的结构简式CH2=CHCH2COOH、CH3CH=CHCOOH、CH2=CHCOOCH3、HCOOCH2CH=CH2、HCOOCH=CHCH3、CH3COOCH=CH2、HCOOC(CH3)=CH2(其中任两种).
结构的D的所有同分异构共有7种(不包括顺反异构体),写出其中任意两种的结构简式CH2=CHCH2COOH、CH3CH=CHCOOH、CH2=CHCOOCH3、HCOOCH2CH=CH2、HCOOCH=CHCH3、CH3COOCH=CH2、HCOOC(CH3)=CH2(其中任两种).