题目内容
2.诺贝尔化学奖获得者乔治•欧拉教授率领团队首次采用金属钌作催化剂,从空气中捕获CO2直接转化为甲醇,为通往未来“甲醇经济”迈出了重要一步,并依据该原理开发如图1所示转化.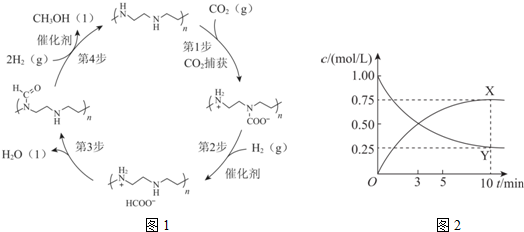
(1)CO2中含有的化学键类型是极性共价键.
(2)将生成的甲醇(沸点为64.7℃)与水分离可采取的方法是蒸馏.
(3)图1所示转化中,由第1步至第4步的反应热(△H)依次是a kJ/mol、b kJ/mol、c kJ/mol、d kJ/mol,则该转化总反应的热化学方程式是CO2(g)+3H2(g)?CH3OH(l)+H2O(l)△H=(a+b+c+d)kJ/mol.
(4)500℃时,利用金属钌做催化剂,在固定容积的密闭容器中可直接实现如(3)中转化得到甲醇.测得该反应体系中X、Y浓度随时间变化如图2.
①Y的化学式是,判断的理由是Y随反应进行浓度减小,因此Y为反应物,且其相同时间内转化量与X相同,则其在方程式中的化学计量数应与X相同,因此Y是CO2.
②下列说法正确的是abc(选填字母).
a.Y的转化率是75%
b.其他条件不变时,若在恒压条件下进行该反应,Y的转化率高于75%
c.升高温度使该反应的平衡常数K增大,则可知该反应为吸热反应
d.金属钌可大大提高该反应中反应物的转化率
③从反应开始到平衡,用氢气表示的平均反应速率v(H2)=0.225mol/(L•min).
分析 (1)CO2中含有极性共价键;
(2)互溶沸点不同的液体混合物用蒸馏的方法分离;
(3)根据盖斯定律,可知反应热的大小与起态和始态有关与过程无关;
(4)①由图可知X的量在增加,Y的量再减少,而且变化量相同,所以Y是反应物,而且计量数与生成物的计量数相同;
②a.Y的转化率是$\frac{1-0.25}{1}×100%$=75%;
b.因为正反应是气体体积减少的反应,所以其他条件不变时,若在恒压条件下进行该反应,相当于增大压强,Y的转化率变大;
c.升高温度使该反应的平衡常数K增大,则可知该反应为吸热反应;
d.催化剂只改变反应的速率,但平衡不移动;
③速率之比等于对应物质的化学计量数之比,结合v=$\frac{△c}{△t}$进行计算.
解答 解:(1)CO2中含有极性共价键,故答案为:极性共价;
(2)甲醇(沸点为64.7℃)与水的沸点不同,所以用蒸馏的方法分离,故答案为:蒸馏;
(3)根据盖斯定律,可知反应热的大小与起态和始态有关与过程无关,所以该转化总反应的热化学方程式是CO2(g)+3H2(g)?CH3OH(l)+H2O(l)△H=(a+b+c+d) kJ/mol,故答案为:CO2(g)+3H2(g)?CH3OH(l)+H2O(l)△H=(a+b+c+d) kJ/mol;
(4)①由图可知X的量在增加,Y的量再减少,而且变化量相同,所以Y是反应物,而且计量数与生成物的计量数相同,所以Y是CO2,故答案为:CO2;Y随反应进行浓度减小,因此Y为反应物,且其相同时间内转化量与X相同,则其在方程式中的化学计量数应与X相同,因此Y是CO2;
②a.Y的转化率是$\frac{1-0.25}{1}×100%$=75%,故正确;
b.因为正反应是气体体积减少的反应,所以其他条件不变时,若在恒压条件下进行该反应,相当于增大压强,Y的转化率变大,故正确;
c.升高温度使该反应的平衡常数K增大,则可知该反应为吸热反应,故正确;
d.催化剂只改变反应的速率,但平衡不移动,故错误;
故选:abc;
③v(CO2)=$\frac{0.75}{10}$=0.075mol/(L•min),而v(H2)=$\frac{1}{3}$v(CO2)=0.225 mol/(L•min),故答案为:0.225.
点评 本题为综合题,涉及化学平衡影响因素分析、化学反应速率的计算、反应热的计算、热化学反应方程式的书写等知识点,注重高考常考考点的考查,题目难度中等.

 ABC考王全优卷系列答案
ABC考王全优卷系列答案| A. | 4,4,3-三甲基己烷 | B. | 2-甲基-4-乙基戊烷 | ||
| C. | 3-甲基-2-戊炔 | D. | 2,2-二甲基戊烷 |
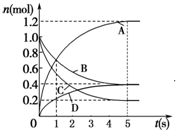 一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )| A. | 该反应的化学方程式为6A+2 D?3B+4C | |
| B. | 反应进行到1 s时,v(A)=v(B) | |
| C. | 反应进行到5 s时,B的平均反应速率为0.06mol/(L•s) | |
| D. | 反应进行到5 s时,v(A)=v(B)=v(C)=v(D) |
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)最高价氧化物的水化物碱性最强的是NaOH,酸性最强的是HClO4,呈两性的是Al(OH)3;
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的HF;
(4)从大到小排列D、E、F最高价氧化物对应水化物的酸性强弱HNO3>H3PO4>H2CO3.
| A. | CO2 | B. | Na2O | C. | MgBr2 | D. | NH4Cl |
| A. | 0.37 | B. | 0.24 | C. | 0.16 | D. | 无法确定 |
| A. | 乙醇和汽油都是可再生能源,应大力推广使用乙醇汽油 | |
| B. | 凡含有食品添加剂的食物对人体健康均有害,不宜食用 | |
| C. | PM2.5主要来自于煤和石油等化石燃料的燃烧 | |
| D. | 汽车尾气中的一氧化氮遇空气在低温下能自发进行反应,说明该反应的△H>O |
| A. | 甲烷不能使酸性高锰酸钾溶液褪色,而甲苯能使酸性高锰酸钾溶液褪色 | |
| B. | 乙醇能发生消去反应,而乙烷不能发生消去反应 | |
| C. | 苯与硝酸在加热的条件下发生取代反应,而甲苯在常温下就能与硝酸发生硝化反应 | |
| D. | 乙烷在光照条件下能发生取代反应,而乙炔不能发生取代反应 |
 、
、 、
、 ..
..