题目内容
2.下列说法中不正确的是( )| A. | 通常情况下,镀锌铁的镀层损坏后,仍然可以保护铁不被腐蚀 | |
| B. | 电镀时,通常把待镀的金属制品作阴极,把镀层金属作阳极 | |
| C. | 化学电池是将化学能变成电能的装置,它包括一次电池、二次电池和燃料电池等几大类 | |
| D. | 粗铜精炼的过程中,用纯铜板作阳极,粗铜板作阴极 |
分析 A.Fe与Zn形成原电池时Fe作正极被保护;
B.电镀时,镀层作阳极、待镀的金属制品作阴极;
C.化学电池是将化学能变成电能的装置,依据化学电池的分类解答;
D.阴极电解原理分析,电解精炼铜粗铜做阳极,精铜做阴极,含铜离子的电解质溶液.
解答 解:A.Fe与Zn形成原电池时Fe作正极被保护,所以镀锌铁的镀层破损后,镀层仍然对铁起保护作用,故A正确;
B.电镀时,阳极上金属失电子发生氧化反应、阴极上金属阳离子得电子发生还原反应生成金属单质,所以镀层作阳极、待镀的金属制品作阴极,故B正确;
C.化学电池是将化学能变成电能的装置,它包括一次电池、二次电池和燃料电池等几大类,故C正确;
D.用电解法精炼粗铜时用纯铜作阴极,粗铜做阳极,故D错误,
故选D.
点评 本题考查了原电池及电解池原理及金属的冶炼,根据金属的活泼性强弱确定冶炼方法,知道原电池和电解池各个电极上发生的反应,难度不大.

练习册系列答案
 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
12.把a mol H2和b mol C2H4混合,在一定条件下使它们一部分发生反应生成w molC2H6,将反应混合气体完全燃烧,余下的C2H4消耗氧气的物质的量为( )
| A. | a+3b | B. | $\frac{a}{2}$+3b | C. | $\frac{a}{2}$+3b+$\frac{7}{2}$ w | D. | 3(b-w) |
13.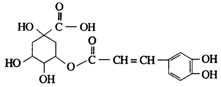 金银花中含有绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法不正确的是( )
金银花中含有绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法不正确的是( )
 金银花中含有绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法不正确的是( )
金银花中含有绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法不正确的是( )| A. | 绿原酸的分子式为C16H8O9 | |
| B. | 1个绿原酸分子中含有4个手性碳原子 | |
| C. | 1mol绿原酸最多与4molNaOH反应 | |
| D. | 1mol绿原酸最多能与6molH2发生反应 |
17.下列叙述不正确的是( )
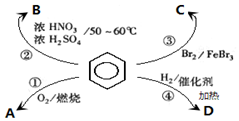

| A. | 反应①为氧化反应,反应现象是火焰明亮并带有浓烟 | |
| B. | 反应②为取代反应,有机产物B是一种芳香烃 | |
| C. | 反应③为取代反应,产物溴苯是比水重的无色液体 | |
| D. | 反应④为加成反应,若H2足量则产物D为环己烷 |
14.下列分散系能产生“丁达尔效应”的是( )
| A. | 苏打水溶液 | B. | 苯酚浊液 | C. | 碘化银胶体 | D. | 氯化钡溶液 |
11.以下转化关系中,元素X、Y是短周期同主族元素,元素Z是过渡元素.

已知:①Z2X、Z2Y不溶于水
②浓硝酸具有强氧化性,反应中常被还原成二氧化氮气体
下列说法不正确的是( )

已知:①Z2X、Z2Y不溶于水
②浓硝酸具有强氧化性,反应中常被还原成二氧化氮气体
下列说法不正确的是( )
| A. | Z2X是Cu2S、Z2Y是Cu2O | |
| B. | 步骤①发生的反应,其离子方程式可能为Cu2S+12H++10NO3ˉ=2Cu2++10NO2↑+SO42ˉ+6H2O | |
| C. | 步骤②发生的反应,其离子方程式为H++OHˉ=H2O、Cu2++2OHˉ=Cu(OH)2↓ | |
| D. | 步骤③发生的反应,说明葡萄糖具有氧化性 |
19.下列物质中,不能由单质直接化合得到的是( )
| A. | FeCl3 | B. | Cu2S | C. | FeS | D. | SO3 |

 .
. 和
和 ⑤
⑤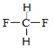 和
和