题目内容
(1)有机化学中,还原反应是指增加 原子或减少 原子;如果碳原子的氧化数为+4时,只能被 ;
(2)1mol分子组成为C3H8O的液态有机物A,与足量的金属钠作用,可生成11.2L氢气(标准状况),则A分子中必有一个 基,若此基团在碳链的一端,则A的结构简式为 ;A与浓硫酸共热,分子内脱去1分子水,生成B,B的结构简式为 ;B通入溴水能发生 反应生成C,C的结构简式为 ;A在有铜作催化剂时,与氧气一起加热,发生氧化反应,生成D,D的结构简式为 .写出下列指定反应的化学方程式
①A→B ;②A→D .
(2)1mol分子组成为C3H8O的液态有机物A,与足量的金属钠作用,可生成11.2L氢气(标准状况),则A分子中必有一个
①A→B
分析:(1)有机物的氧化反应是指得氧、失氢,还原反应是指得氢、失氧;
(2)n(H2)=
=0.5mol,该有机物丙醇,若羟基在碳链的一端,应为CH3CH2CH2OH,在浓硫酸作用下可生成CH3CH=CH2,与溴水发生加成反应可生成CH3CHBrCH2Br,发生催化氧化可生成CH3CH2CHO,以此解答该题.
(2)n(H2)=
| 11.2L |
| 22.4L/mol |
解答:解:(1)有机化学中,还原反应是指增加氢原子或减少氧原子,如果碳原子的氧化数为+4时,只能被还原,故答案为:H;O;还原;
(2)1mol分子组成为C3H8O的液态有机物A,与足量的金属钠作用,可生成11.2L氢气,n(H2)=
=0.5mol,该有机物丙醇,含有1个-OH,若羟基在碳链的一端,应为CH3CH2CH2OH,在浓硫酸作用下可生成CH3CH=CH2,反应的方程式为CH3CH2CH2OH
CH3CH=CH2+H2O,与溴水发生加成反应可生成CH3CHBrCH2Br,发生催化氧化可生成CH3CH2CHO,反应的方程式为2CH3CH2CH2OH+O2
2CH3CH2CHO+2H2O,
故答案为:羟;CH3CH2CH2OH;CH3CH=CH2;加成;CH3CHBrCH2Br;CH3CH2CHO;CH3CH2CH2OH
CH3CH=CH2+H2O;2CH3CH2CH2OH+O2
2CH3CH2CHO+2H2O.
(2)1mol分子组成为C3H8O的液态有机物A,与足量的金属钠作用,可生成11.2L氢气,n(H2)=
| 11.2L |
| 22.4L/mol |
| 浓硫酸 |
| △ |
| Cu |
| △ |
故答案为:羟;CH3CH2CH2OH;CH3CH=CH2;加成;CH3CHBrCH2Br;CH3CH2CHO;CH3CH2CH2OH
| 浓硫酸 |
| △ |
| Cu |
| △ |
点评:本题考查有机物的推断,题目难度中等,注意根据有机物的化学式以及相关性质进行推断,注意了解有机物发生氧化还原反应的特点.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
 结构的有机物可被碱性高锰酸钾氧化成二元醇,如:CH2═CH2
结构的有机物可被碱性高锰酸钾氧化成二元醇,如:CH2═CH2 HOCH2CH2OH,现以2一甲基丙烯为原料合成环状化台物F和高分子化合物E和G.
HOCH2CH2OH,现以2一甲基丙烯为原料合成环状化台物F和高分子化合物E和G.








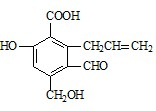
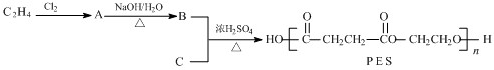


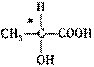 )。在有机化学中,还引入不饱和度,也称缺氢指数(用Ω表示)。分子中每减少2个氢原子(意味着分子中有1个双键或1个环)Ω=1。例如:2-丁烯的Ω=1;
)。在有机化学中,还引入不饱和度,也称缺氢指数(用Ω表示)。分子中每减少2个氢原子(意味着分子中有1个双键或1个环)Ω=1。例如:2-丁烯的Ω=1;