题目内容
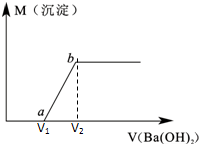 某溶液由盐酸、Na2CO3、H2SO4、CuCl2四种物质中的一种或几种混合形成,现向该混合溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图所示.
某溶液由盐酸、Na2CO3、H2SO4、CuCl2四种物质中的一种或几种混合形成,现向该混合溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图所示.(1)该溶液中一定含
(2)写出图中a点之前的离子方程式:
写出图中a→b点的离子方程式:
(3)将所得沉淀进行过滤,洗涤,干燥,称量,应如何判断沉淀是否完全洗净:
(4)若b点时沉淀质量=2.94克,V1=20mL,V2=40mL,求cBa(OH)2=
考点:离子方程式的有关计算
专题:计算题,离子反应专题
分析:由图象可知,加Ba(OH)2溶液V1ml时,没有沉淀生成,说明Ba(OH)2与HCl反应,则含有HCl,能与HCl反应的物质不存在,则不存在Na2CO3,H2SO4与Ba(OH)2反应生成硫酸钡沉淀,硫酸钡不容易酸,所以一开始会产生沉淀与图象不符,则没有H2SO4,V1ml后有沉淀生成,说明有CuCl2;
(1)根据以上分析判断;
(2)a点之前为盐酸与氢氧化钡反应;a→b点为CuCl2与Ba(OH)2反应;
(3)溶液中含有氯离子,检验滤液中是否含有氯离子即可;
(4)根据发生的离子方程式计算.
(1)根据以上分析判断;
(2)a点之前为盐酸与氢氧化钡反应;a→b点为CuCl2与Ba(OH)2反应;
(3)溶液中含有氯离子,检验滤液中是否含有氯离子即可;
(4)根据发生的离子方程式计算.
解答:
解:由图象可知,加Ba(OH)2溶液V1ml时,没有沉淀生成,说明Ba(OH)2与HCl反应,则含有HCl,能与HCl反应的物质不存在,则不存在Na2CO3,H2SO4与Ba(OH)2反应生成硫酸钡沉淀,硫酸钡不容易酸,所以一开始会产生沉淀与图象不符,则没有H2SO4,V1ml后有沉淀生成,说明有CuCl2;
(1)该溶液中一定含HCl,CuCl2;故答案为:HCl,CuCl2;
(2)a点之前为盐酸与氢氧化钡反应,则其反应的离子方程式为:H++OH-═H2O;a→b点为CuCl2与Ba(OH)2反应,其反应的离子方程式为:Cu2++2OH-═Cu(OH)2↓;
故答案为:H++OH-═H2O;Cu2++2OH-═Cu(OH)2↓;
(3)溶液中含有氯离子,则沉淀上会附着氯离子,则检验滤液中是否含有氯离子即可判断沉淀是否洗涤干净,则操作为:取最后一次洗涤液少许,加入酸化AgNO3,若无沉淀,则已洗净;
故答案为:取最后一次洗涤液少许,加入酸化AgNO3,若无沉淀,则已洗净;
(4)若b点时沉淀质量=2.94克,则Cu(OH)2的物质的量为
=0.03mol,
Cu2++2OH-═Cu(OH)2↓
则与CuCl2反应的Ba(OH)2为0.03mol,其体积为40ml-20ml=20ml=0.02L,
所以cBa(OH)2=
=1.5mol/L;
故答案为:1.5mol/L.
(1)该溶液中一定含HCl,CuCl2;故答案为:HCl,CuCl2;
(2)a点之前为盐酸与氢氧化钡反应,则其反应的离子方程式为:H++OH-═H2O;a→b点为CuCl2与Ba(OH)2反应,其反应的离子方程式为:Cu2++2OH-═Cu(OH)2↓;
故答案为:H++OH-═H2O;Cu2++2OH-═Cu(OH)2↓;
(3)溶液中含有氯离子,则沉淀上会附着氯离子,则检验滤液中是否含有氯离子即可判断沉淀是否洗涤干净,则操作为:取最后一次洗涤液少许,加入酸化AgNO3,若无沉淀,则已洗净;
故答案为:取最后一次洗涤液少许,加入酸化AgNO3,若无沉淀,则已洗净;
(4)若b点时沉淀质量=2.94克,则Cu(OH)2的物质的量为
| 2.94g |
| 98g/mol |
Cu2++2OH-═Cu(OH)2↓
则与CuCl2反应的Ba(OH)2为0.03mol,其体积为40ml-20ml=20ml=0.02L,
所以cBa(OH)2=
| 0.03mol |
| 0.02L |
故答案为:1.5mol/L.
点评:本题考查了物质的检验、离子反应、物质的量的有关计算,题目涉及的知识点较多,侧重于考查学生对基础知识的应用能力,题目难度中等.

练习册系列答案
相关题目
设NA表示阿伏加德罗常数的数值,下列叙述中正确的是( )
| A、常温常压下,48gO3含有的氧原子数为NA个 |
| B、24g金属镁变为镁离子时失去的电子数为NA个 |
| C、在0℃、101kP时,28gN2和CO的混合气体,其体积约为22.4L |
| D、同温同压下,NA个NO与NA个N2和O2的混合气体的体积不相等 |
已知反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ?mol-1和2H2(g)+O2(g)═2H2O(g)△H=-484kJ?mol-1.则下列说法不正确的是( )
| A、CO转化为CO2的热化学方程式为2CO(g)+O2(g)═2CO2(g)△H=-566 kJ?mol-1 | ||
B、CO燃烧热的热化学方程式为CO(g)+
| ||
| C、放热反应可能需要加热才能进行,而吸热反应一定需要加热才能进行 | ||
| D、1mol H2完全燃烧生成1mol 液态水,放出的热量大于242 kJ |
下列说法正确的是( )
| A、纯净物一定由分子构成 |
| B、同种分子构成的物质一定是纯净物 |
| C、混合物肯定由两种以上元素组成 |
| D、盐中一定含有金属元素 |
下列中和反应对应的离子方程式能以“H++OH-═H2O”表示的是( )
| A、醋酸和氢氧化钠溶液反应 |
| B、氢氧化镁和盐酸反应 |
| C、澄清石灰水和硝酸反应 |
| D、氢氧化钡和稀硫酸反应 |
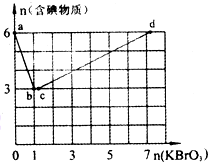 现向含6 mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加人KBrO3的物质的量的关系如图所示.请回答下列问题:
现向含6 mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加人KBrO3的物质的量的关系如图所示.请回答下列问题: