题目内容
将0.15mol MnO2和50ml 12mol·L-1浓盐酸混合后缓慢加热,充分反应可制得氯气的物质的量为( )
A.等于0.15mol B.大于0.15mol C.小于0.15mol D.以上结论都不对
【答案】
C
【解析】
试题分析:氯化氢的物质的量是0.05L×12mol/L=0.6mol,根据反应的方程式MnO2+4HCl(浓)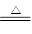 MnCl2+2H2O+Cl2↑可知,反应物恰好反应,生成0.15mol氯气。但由于在反应过程中,盐酸的浓度会逐渐降低,而稀盐酸不能被氧化,所以实际生成的氯气小于0.15mol,答案选C。
MnCl2+2H2O+Cl2↑可知,反应物恰好反应,生成0.15mol氯气。但由于在反应过程中,盐酸的浓度会逐渐降低,而稀盐酸不能被氧化,所以实际生成的氯气小于0.15mol,答案选C。
考点:考查二氧化锰和浓盐酸反应的有关计算
点评:与该题类似的还有铜和浓硫酸的反应、以及金属和浓硝酸的反应。都是由于反应物的浓度降低,要么生成物发生变化,要么是生成物的实际数值偏小等,在进行有关的计算时,需要注意。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将10ml 0.2mol/L的含氧酸HxRO4 与20ml 0.15mol/L的某碱M(OH)a溶液恰好完全反应,则R的化合价为()
| A.+4 | B.+6 | C.8-1.5a | D.8-3a |