题目内容
4.下列有关实验操作的说法正确的是( )| A. | 用10mL量筒量取8.10mL稀盐酸 | |
| B. | 可用25mL酸式滴定管量取20.00mL KMnO4溶液 | |
| C. | 用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸 | |
| D. | 用pH计测得某溶液的pH为2 |
分析 A.量筒的感量为0.1mL;
B.酸式滴定管的感量为0.01mL;
C.pH试纸不能湿润;
D.pH计测定值准确到小数点后一位数.
解答 解:A.量筒的感量为0.1mL,则用10mL量筒量取8.1mL稀盐酸,故A错误;
B.酸式滴定管的感量为0.01mL,则用25mL酸式滴定管量取20.00mL KMnO4溶液,故B正确;
C.pH试纸不能湿润,选干燥的pH试纸测定溶液的pH,故C错误;
D.pH计测定值准确到小数点后一位数,不能为正整数,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握仪器的使用、pH的测定、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
15.二氧化硫是硫的重要化合物,在生产、生活中有广泛应用.二氧化硫有毒,并且是形成酸雨的主要气体.无论是实验室制备还是工业生产,二氧化硫尾气吸收或烟气脱硫都非常重要.完成下列填空:
(1)实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫.实验室二氧化硫尾气吸收与工业烟气脱硫的化学原理相通.
石灰-石膏法和碱法是常用的烟气脱硫法.
石灰-石膏法的吸收反应为:SO2+Ca(OH)2═CaSO3↓+H2O.吸收产物亚硫酸钙由管道输送至氧化塔氧化,
反应为2CaSO3+O2+4H2O=2CaSO4•2H2O.其流程如图: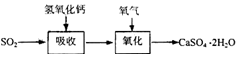
碱法的吸收反应为SO2+2NaOH=Na2SO3+H2O.碱法的特点是氢氧化钠碱性强、吸收快、效率高.
其流程如图: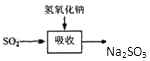
已知:
(1)石灰-石膏法和碱法吸收二氧化硫的化学原理相同之处是利用SO2是酸性氧化物,可与碱反应.和碱法相比,石灰-石膏法的优点是原料易得,吸收成本低.
(2)在石灰-石膏法和碱法的基础上,设计一个改进的、能实现物料循环的烟气脱硫方案(用流程图表示).
(1)实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫.实验室二氧化硫尾气吸收与工业烟气脱硫的化学原理相通.
石灰-石膏法和碱法是常用的烟气脱硫法.
石灰-石膏法的吸收反应为:SO2+Ca(OH)2═CaSO3↓+H2O.吸收产物亚硫酸钙由管道输送至氧化塔氧化,
反应为2CaSO3+O2+4H2O=2CaSO4•2H2O.其流程如图:

碱法的吸收反应为SO2+2NaOH=Na2SO3+H2O.碱法的特点是氢氧化钠碱性强、吸收快、效率高.
其流程如图:

已知:
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 0.36 | 2.9 |
| 吸收SO2的成本(元/mol) | 0.027 | 0.232 |
(2)在石灰-石膏法和碱法的基础上,设计一个改进的、能实现物料循环的烟气脱硫方案(用流程图表示).
12. 已知25℃时部分弱电解质的电离平衡常数数据如表:
已知25℃时部分弱电解质的电离平衡常数数据如表:
(1)等物质的量浓度的 a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的pH由大到小的顺序为cbda(填字母).
(2)常温下,0.1mol•L-1的CH3COOH 溶液加水稀释,下列表达式的数据变大的是B.
A.C(H+) B.C(H+)/C(CH3COOH) C.C(H+)•C(OH-)
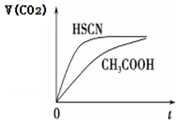
(3)25℃时,将 20mL 0.1mol•L-1 CH3COOH 溶液和 20mL0.1mol•L-1HSCN溶液分别与20mL 0.1mol•L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示:反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快; 反应结束后所得两溶液中,(CH3COO-)<c(SCN-)(填“>”、“<”或“=”)
(4)25℃时,在 CH3COOH 与 CH3COONa 的混合溶液中,若测得 pH=6,则溶液中c(CH3COO-)-c(Na+)=9.9×10-7mol•L-1(填精确值),c(CH3COO-)/c(CH3COOH)=17.
(5)用离子方程式表示Na2CO3溶液呈碱性的原因CO32-+H2O?HCO3-+OH-.
 已知25℃时部分弱电解质的电离平衡常数数据如表:
已知25℃时部分弱电解质的电离平衡常数数据如表:| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.7×10-5 | 6.2×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
(2)常温下,0.1mol•L-1的CH3COOH 溶液加水稀释,下列表达式的数据变大的是B.
A.C(H+) B.C(H+)/C(CH3COOH) C.C(H+)•C(OH-)
(3)25℃时,将 20mL 0.1mol•L-1 CH3COOH 溶液和 20mL0.1mol•L-1HSCN溶液分别与20mL 0.1mol•L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示:反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快; 反应结束后所得两溶液中,(CH3COO-)<c(SCN-)(填“>”、“<”或“=”)
(4)25℃时,在 CH3COOH 与 CH3COONa 的混合溶液中,若测得 pH=6,则溶液中c(CH3COO-)-c(Na+)=9.9×10-7mol•L-1(填精确值),c(CH3COO-)/c(CH3COOH)=17.
(5)用离子方程式表示Na2CO3溶液呈碱性的原因CO32-+H2O?HCO3-+OH-.
9. 在密闭容器中发生反应:X+2Y?2Z(△H<0),其中Z显气态,且Z在平衡混合气中的体积分数(Z%)与温度(T)、压强(P)的关系如图,下列判断正确的是( )
在密闭容器中发生反应:X+2Y?2Z(△H<0),其中Z显气态,且Z在平衡混合气中的体积分数(Z%)与温度(T)、压强(P)的关系如图,下列判断正确的是( )
 在密闭容器中发生反应:X+2Y?2Z(△H<0),其中Z显气态,且Z在平衡混合气中的体积分数(Z%)与温度(T)、压强(P)的关系如图,下列判断正确的是( )
在密闭容器中发生反应:X+2Y?2Z(△H<0),其中Z显气态,且Z在平衡混合气中的体积分数(Z%)与温度(T)、压强(P)的关系如图,下列判断正确的是( )| A. | Y一定呈气态 | |
| B. | T1大于T2 | |
| C. | 升高温度,该反应的化学平衡常数增大 | |
| D. | 当c(X):c(Y):c(Z)=1:2:2时,反应达到平衡状态 |
16.在给定条件下,下列选项所示的物质间转化均能实现的是( )
| A. | N2$→_{放电}^{O_{2}}$NO$\stackrel{H_{2}O}{→}$HNO3 | |
| B. | MnO2$→_{△}^{浓硫酸}$Cl2$\stackrel{石灰乳}{→}$漂白粉 | |
| C. | 黄铁矿$\stackrel{沸腾炉}{→}$SO3$→_{水}^{吸收塔}$硫酸 | |
| D. | CuSO4(aq) $\stackrel{NaOH溶液}{→}$Cu(OH)2$→_{△}^{蔗糖}$Cu2O |
13.下列气体通入水中所得溶液呈碱性的是( )
| A. | CO2 | B. | SO2 | C. | NH3 | D. | HC1 |
14.下列说法正确的是( )
| A. | 向Al2(SO4)3溶液中加入过量的NH3•H2O:Al3++4NH3•H2O═[Al(OH)4]-+4NH4+ | |
| B. | 检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可用KMnO4溶液 | |
| C. | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来,金属铝的熔点较低 | |
| D. | 将铜粉加1.0 mol•L-1Fe2(SO4)3溶液中,溶液变蓝,有黑色固体出现,说明金属铁比铜活泼 |