题目内容
9.下列说法正确的是( )| A. | pH=3的盐酸与pH=11的氨水等体积混合后,溶液中:c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| B. | 升高NH4Cl溶液的温度,其水的离子积常数和pH均增大 | |
| C. | 反应2Mg(s)+CO2(g)═C(s)+2MgO(s)能自发进行,则该反应的△H>0 | |
| D. | 常温下0.1mol/L的Na2A溶液pH=10,该溶液中水电离的c(OH-)=10-10mol/L |
分析 A.pH=3的盐酸与pH=11的氨水等体积混合后,氨水浓度大,溶质为氯化铵、一水合氨,电离显碱性;
B.水的电离、盐类水解均吸热,加热促进水解;
C.△H-T△S<0的反应可自发进行;
D.0.1mol/L的Na2A溶液pH=10,可知阴离子水解显碱性,促进水的电离.
解答 解:A.pH=3的盐酸与pH=11的氨水等体积混合后,氨水浓度大,溶质为氯化铵、一水合氨,电离显碱性,则离子浓度为c(NH4+)>c(Cl-)>c(OH-)>c(H+),故A正确;
B.水的电离、盐类水解均吸热,加热促进水解,则升高温度,水的离子积增大,pH减小,故B错误;
C.△H-T△S<0的反应可自发进行,反应的△S<0,能自发进行,可知该反应的△H<0,故C错误;
D.0.1mol/L的Na2A溶液pH=10,可知阴离子水解显碱性,促进水的电离,则该溶液中水电离的c(OH-)=10-4mol/L,故D错误;
故选A.
点评 本题考查离子浓度大小的比较,为高频考点,把握酸碱混合后溶液的溶质、盐类水解、弱电解质的电离为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.

练习册系列答案
相关题目
19.已知:C(s)+O2(g)=CO2(g)△H1
CO2(g)+C(s)=2CO(g)△H2
2CO(g)+O2(g)=2CO2(g)△H3
4Fe(s)+3O2(g)=2Fe2O3(s)△H4
3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
CO2(g)+C(s)=2CO(g)△H2
2CO(g)+O2(g)=2CO2(g)△H3
4Fe(s)+3O2(g)=2Fe2O3(s)△H4
3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
| A. | 2△H1>△H3 | B. | △H3=△H4+△H5 | C. | △H1=△H2+△H3 | D. | △H2<0,△H4<0 |
20.如表所示是元素周期表示意图的一部分,根据表中10种元素,用元素符号或化学式填空.
(1)①~⑩元素中,金属性最强的是K(填元素符号).
(2)①~⑩元素中,最高价氧化物对应的水化物呈两性的元素是Al(填元素符号),该最高价氧化物对应的水化物与NaOH溶液反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O
(3)①~⑩元素中,最高价氧化物对应的水化物的酸性最强的是HClO4(填化学式),碱性最强的是KOH(填化学式).
(4)⑤、⑥、⑧、⑨所形成的简单离子的半径由大到小的顺序是S2->Cl->K+>Ca2+.(填离子符号)
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 4 | ⑧ | ⑨ | ⑩ |
(2)①~⑩元素中,最高价氧化物对应的水化物呈两性的元素是Al(填元素符号),该最高价氧化物对应的水化物与NaOH溶液反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O
(3)①~⑩元素中,最高价氧化物对应的水化物的酸性最强的是HClO4(填化学式),碱性最强的是KOH(填化学式).
(4)⑤、⑥、⑧、⑨所形成的简单离子的半径由大到小的顺序是S2->Cl->K+>Ca2+.(填离子符号)
17.W、X、Y、Z为原子序数依次增大的短周期主族元素,W的原子核外只有6个电子,X+和Y3+的电子层结构相同,Z-的电子数比Y3+多8个,下列叙述正确的是( )
| A. | W在自然界只有一种核素 | |
| B. | 半径大小:X+<Y3+<Z- | |
| C. | Y与Z形成的化合物的水溶液呈弱酸性 | |
| D. | X的最高价氧化物对应的水化物为弱碱 |
4.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1molCl2与足量Fe反应转移电子数一定为3NA | |
| B. | 标准状况下,2.24LNH3中含有共价键的数目为NA | |
| C. | 标况下,11.2LSO3所含的分子数目为0.5NA | |
| D. | lmolNa2O和Na2O2混合物中含有的阴、阳离子总数是3NA |
14.实验室拟制备纯净的氯气并回收剩余药品,下列图示装置和原理能达到实验目的是( )
| A. |  制备Cl2 | B. | 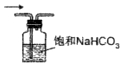 去除杂质 | C. |  干燥Cl2 | D. |  回收固体MnO2 |
1.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 0.1 mol的白磷(P4)或甲烷中所含的共价键数均为0.4NA | |
| B. | 将1 mol Cl2通入水中,HC1O、Cl-、ClO-粒子数之和为2NA | |
| C. | 6.4 g由S2、S4、S8组成的混合物含硫原子数为0.2NA | |
| D. | 密闭容器中2 mol NO与1 mol O2充分反应后,产物的分子数为NA |
2.NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,4 g H2含有的分子数为 2NA | |
| B. | 8 g H2O在标准状况下的体积是22.4 L | |
| C. | 2.3 g金属钠变为钠离子时失去的电子数为NA | |
| D. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA |
3.中华传统文化博大精深,其中涉及到很多的化学知识.下列有关说法不正确的是( )
| A. | 中国的圆珠笔头一直需要进口笔尖钢,经过5 年数不清的失败,2016年9月,中国太钢集团利用家常和面原理在钢水中加入添加剂试验成功,造出圆珠笔头,可完全替代进口,由此信息可知笔尖钢为合金,且具有良好的切削性 | |
| B. | 工业生产玻璃、水泥、漂白粉,均需要用石灰石为原料 | |
| C. | 《天工开物》中有“至于矾现五色之形,硫为群石之将,皆变化于烈火”,其中的矾指的是金属硫化物 | |
| D. | 中国蓝是古代人工合成的蓝色化合物,其化学式为BaCuSi4O10,可改写成BaO•CuO•4SiO2 |