题目内容
10.下列有关过氧化氢的叙述中不正确的是( )| A. | 氧原子采取的是sp2杂化 | B. | 分子中有3个σ键 | ||
| C. | 过氧化氢是极性分子 | D. | 每个氧原子上有两个孤对电子对 |
分析 过氧化氢(H2O2)分子的空间结构示意图为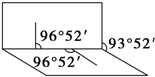 ,由H2O2的结构可知,O原子形成1个O-H键、1个O-O键,含有2对孤对电子,杂化轨道数为4,杂化方式为sp3,且分子结构不对称,为极性分子,以此解答该题.
,由H2O2的结构可知,O原子形成1个O-H键、1个O-O键,含有2对孤对电子,杂化轨道数为4,杂化方式为sp3,且分子结构不对称,为极性分子,以此解答该题.
解答 解:A.O原子形成1个O-H键、1个O-O键,含有2对孤对电子,杂化轨道数为4,杂化方式为sp3,故A错误;
B.分子中含有2个O-H键、1个O-O键,则分子中有3个σ键,故B正确;
C.分子结构不对称,正负电荷重心不重叠,为极性分子,故C正确;
D.过氧化氢的电子式为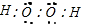 ,可知每个氧原子上有两个孤对电子对,故D正确.
,可知每个氧原子上有两个孤对电子对,故D正确.
故选A.
点评 本题以过氧化氢为载体综合考查化学键的形成方式及键的极性和分子的极性判断等知识,为高频考点,侧重考查学生的分析能力,要注意基础知识的积累,难度不大.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
1.下列关于烷烃的叙述中不正确的是( )
| A. | 在烷烃分子中,所有的化学键都为单键 | |
| B. | 所有的烷烃在一定条件下都能与Cl2发生取代反应 | |
| C. | 随着碳原子数的增加,烷烃的熔、沸点逐渐升高 | |
| D. | 任何烷烃分子中碳氢原子个数之比都是相同的 |
18.下列有关元素周期表的说法不正确的是( )
| A. | 元素周期表共有16个族 | B. | 元素周期表含元素最多的是第ⅢB族 | ||
| C. | 第ⅡA族与第ⅢA族不相邻 | D. | 第ⅠA族元素又称为碱金属元素 |
5.下列各种情况下,埋在地下的铸铁输气管道被腐蚀的速度最慢的是( )
| A. | 在干燥、致密、不透气的土壤中 | B. | 在潮湿、疏松、透气的土壤中 | ||
| C. | 在呈酸性的潮湿土壤中 | D. | 在含沙粒较多、潮湿的土壤中 |
15.某学生将电流表用导线与两个电极连接在一起,再将两个电极同时插入某种电解质溶液中,能观察到有电流产生的是( )
| A. | 用铜片、铅笔芯作电极插入稀硫酸中 | |
| B. | 用两个铜片作电极插入硝酸银溶液中 | |
| C. | 用锌片、铜片作电极插入酒精中 | |
| D. | 用铜片、铁片作电极插入柠檬汁中 |
2.下列各反应中,符合图所示能量变化的是( )


| A. | H2和Cl2的反应 | B. | Al和盐酸的反应 | ||
| C. | CaO和H2O的反应 | D. | Ba(OH)2•8H2O和NH4Cl的反应 |
19.有甲、乙两位同学,他们一起做了水果电池的实验,测得的数据如表:
下列叙述中不正确的是( )
| 实验序号 | 电极材料 | 水果品种 | 电极间距/cm | 电压/mV | |
| 1 | 锌 | 铜 | 菠萝 | 3 | 900 |
| 2 | 锌 | 铝 | 菠萝 | 3 | 650 |
| 3 | 锌 | 铝 | 苹果 | 3 | 450 |
| A. | 实验l 中锌为负极,电子由锌经导线流向铜 | |
| B. | 实验2 中铝为负极,铝失去电子,电流由锌经导线流向铝 | |
| C. | 实验3 中铝为负极,电极反应为Al-3e-═A13+ | |
| D. | 水果电池的电压只跟水果的品种有关 |
18.为了提纯表所列物质(括号内为杂质),有关除杂试剂和分离方法的选择均不正确的是( )
| 编号 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 乙烷(乙烯) | 溴水 | 洗气 |
| B | 淀粉溶液(NaCl) | 水 | 过滤 |
| C | 乙醇(水) | CaO | 蒸馏 |
| D | 乙酸乙酯(乙酸) | 饱和Na2CO3溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |