题目内容
1.已知反应Na2SO4•10H2O═Na2SO4•nH2O+(10-n)H2O.有人设想将芒哨(Na2SO4•10H2O)密封在聚乙烯管中,然后将该管安装在房屋的外墙内,使其白天蓄热致室内保持低温度,晚上再把白天所蓄热量放出,使室内保持温暖.对该设想,下列说法中的正确是( )| A. | 晚上发生的是放热反应 | B. | 白天将化学能转化为太阳能 | ||
| C. | 晚上将化学能转化为热能 | D. | 此法可减少温室气体的排放 |
分析 Na2SO4•10H2O═Na2SO4•nH2O+(10-n)H2O,白天白天蓄热致室内保持低温度,可说明分解为吸热反应,晚上再把白天所蓄热量放出,Na2SO4•nH2O、(10-n)H2O可生成Na2SO4•10H2O,为放热反应,以此解答该题.
解答 解:A.晚上再把白天所蓄热量放出,为放热反应,故A正确;
B.白天蓄热致室内保持低温度,说明吸收热量,太阳能转化为化学能,故B错误;
C.晚上再把白天所蓄热量放出,释放热量,将化学能转化为热能,故C正确;
D.与二氧化碳无关,不能减少温室效应,故D错误.
故选AC.
点评 本题考查化学反应与能量变化,为高频考点,侧重考查学生的分析能力,注意把握能量的变化以及反应的关系,难度不大.

练习册系列答案
相关题目
12.下列有关有机物的叙述不正确的是( )
| A. | C5H12O的醇有8种结构 | B. | 分子式为C4H8的链烃有2种 | ||
| C. | C4H8O2的酯有4种结构 | D. | C9H12含苯环的烃有8种 |
9.高氯酸是一种酸性极强的无机含氧酸,可用于制备高氯酸盐、人造金刚石提纯等方面.查阅资料得到以下有关高氯酸的信息:
工业上生产高氯酸的同时还生产了亚氯酸钠,工业流程如图:
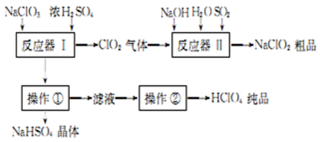
(1)操作①的名称是过滤,操作②的名称是蒸馏.
(2)反应器Ⅰ中发生反应的化学方程式为3NaClO3+3H2SO4=HClO4+2ClO2↑+3NaHSO4+H2O.
(3)反应器Ⅱ中发生反应的离子方程式为4OH-+SO2+2ClO2=2ClO2-+SO42-+2H2O.
(4)若反应器Ⅱ中SO2以H2O2代替也可达到同样的目,此时发生反应的离子方程式为2ClO2+2OH-+H2O2=2ClO2-+O2+2H2O.
(5)若想得到201 kg的 HClO4纯品,至少需要NaClO3 639 kg.
(6)工业上也可用铂作阳极、铜作阴极电解盐酸制得高氯酸,在阳极区可得到20%的高氯酸.写出阳极的电极反应式(其中盐酸与高氯酸以化学式出现)HCl+4H2O-8e-=HClO4+8H+.
| 名称 | 分子式 | 外观 | 沸点 |
| 高氯酸 | HClO4 | 无色液体 | 130℃ |

(1)操作①的名称是过滤,操作②的名称是蒸馏.
(2)反应器Ⅰ中发生反应的化学方程式为3NaClO3+3H2SO4=HClO4+2ClO2↑+3NaHSO4+H2O.
(3)反应器Ⅱ中发生反应的离子方程式为4OH-+SO2+2ClO2=2ClO2-+SO42-+2H2O.
(4)若反应器Ⅱ中SO2以H2O2代替也可达到同样的目,此时发生反应的离子方程式为2ClO2+2OH-+H2O2=2ClO2-+O2+2H2O.
(5)若想得到201 kg的 HClO4纯品,至少需要NaClO3 639 kg.
(6)工业上也可用铂作阳极、铜作阴极电解盐酸制得高氯酸,在阳极区可得到20%的高氯酸.写出阳极的电极反应式(其中盐酸与高氯酸以化学式出现)HCl+4H2O-8e-=HClO4+8H+.
16.国外宇航员吃着“牙膏和砖块”时,中国宇航员已经在太空泡茶了,每个茶装在特制包装袋中,注水后用加热器进行加热就可以喝了,但要插上吸管以防止水珠飘起来,下列说法正确的是( )
| A. | 字航员喝茶时注入的H2O的摩尔质量是18克 | |
| B. | H2O+Cl2?HCl+HClO这反应属于氧化还原反应 | |
| C. | 氢的三种同位素1H、2D、3T与18O只能形成三种水分子 | |
| D. | 在标准状况下,1mol水的体积约是22.4L |
11.下列说法中,正确的是( )
| A. | 化学反应速率是指一定时间内任何一种反应物的物质的量的减少或任何一种生成物物质的量的增加 | |
| B. | 化学反应速率为0.8mol•L-1•s-1是指1秒钟时某物质的浓度为0.8mol•L-1 | |
| C. | 根据化学反应速率的大小可以知道化学反应进行的快慢 | |
| D. | 对于任何化学反应来说,反应速率越快,反应现象就越明显 |
9.下列反应中,不属于取代反应的是( )
| A. | 苯与液溴在FeBr3催化作用下生成溴苯的反应 | |
| B. | 丙烯和氯气在一定条件下反应生成ClCH2CH=CH2 | |
| C. | 乙酸与乙醇生成乙酸乙酯的反应 | |
| D. | 乙烯与HCl气体反应生成一氯乙烷的反应 |