题目内容
2.NA表示阿伏伽德罗常数的值,下列说法正确的是( )| A. | 6.4gCu在足量的硫蒸气中燃烧,转移的电子数为0.1NA | |
| B. | 标准状况下,11.2LSO2和SO3的混合物中硫原子数为0.5NA | |
| C. | 1L0.1mol•L-1的NH4Cl溶液中NH4+数目为0.1NA | |
| D. | 通常情况下,3.4gNH3中共用电子对数为0.8NA |
分析 A.铜与硫单质反应生成的是氯化亚铜;
B.标准状况下三氧化硫的状态不是气体;
C.铵根离子在溶液中发生水解,导致铵根离子数目减少;
D.氨气分子中只含有3个N-H共用电子对.
解答 解:A.6.4g铜的物质的量为:$\frac{6.4g}{64g/mol}$=0.1mol,0.1molCu与硫蒸气反应生成0.05molCu2S,产物中Cu元素的化合价为+1价,则反应中转移电子的物质的量为0.1mol,转移的电子数为0.1NA,故A正确;
B.标准状况下,SO3的状态不是气体吧,不能使用标准状况下的气体摩尔体积计算,故B错误;
C.1L0.1mol•L-1的NH4Cl溶液中含有溶质氯化铵的物质的量为:0.1mol/L×1L=0.1mol,由于部分铵根离子水解,则溶液中含有NH4+数目小于0.1NA,故C错误;
D.3.4g氨气的物质的量为:$\frac{3.4g}{17g/mol}$=0.2mol,0.2mol氨气分子中含有共用电子对的物质的量为:0.2mol×3=0.6mol,含有共用电子对数为0.6NA,故D错误;
故选A.
点评 本题考查了阿伏伽德罗常数的计算与判断,题目难度中等,明确标准状况下气体摩尔体积的使用条件为解答关键,注意熟练掌握物质的量与阿伏伽德罗常数、摩尔质量之间的关系,试题培养了学生的灵活应用能力.

练习册系列答案
 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
12.下列叙述错误的是( )
| A. | 用水可区分苯和溴苯 | |
| B. | 用高锰酸钾酸性溶液可区分己烷和3-己烯 | |
| C. | 用新制的银氨溶液可区分甲酸甲酯和乙醛 | |
| D. | 用金属钠可区分乙醇和乙醚 |
13.某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验.
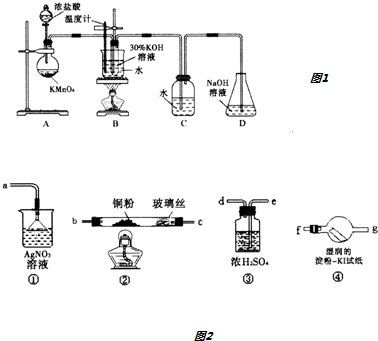
【实验一】制取氯酸钾和氯水.
利用如图1所示实验装置和药品进行实验.
(1)装置A中玻璃仪器为圆底烧瓶和分液漏斗,若对调B和C装置的位置,可能(填“可能”或“不可能”)提高B中氯酸钾的产率.
【实验二】检验上述制备Cl2中混有的HCl.
选用图1装置A和图2所给装置以及药品进行实验.
(2)实验仪器接口连接顺序为:装置A→e、d→b、c→f、g→a.
能证明HCl存在的现象是④中淀粉-KI试纸不变蓝色,装置①中产生白色沉淀.
【实验三】氯酸钾与碘化钾反应的研究.
在不同条件下KClO3可将KI氧化为I2或KIO3.该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
(3)系列a实验的实验目的是研究反应体系中硫酸浓度对反应产物的影响,设计1号试管实验的作用是硫酸浓度为0的对比实验.
【实验四】比较HClO与HCO3-电离常数的大小和测定饱和氯水中氯元素的总量.
查阅资料知:
i.实验室难以获得纯HClO溶液;
ii.次氯酸会破坏酸碱指示剂;
iii.次氯酸或氯气可被SO2、H2O2、和FeCl2等物质还原成Cl-.
(4)设计实验证明(实验方案不必描述操作过程的细节);
①相同条件下,HClO的电离常数大于HCO3-:配制相同物质的量浓度的碳酸钠和次氯酸钠溶液,用pH计分别测定两种溶液的pH值.
②确定饱和氯水中氯元素的总量:量取一定量的试样,加入足量的双氧水溶液,充分反应后,加热除去过量的双氧水,冷却,再加入足量的硝酸银溶液,过滤,洗净烘干后称量沉淀质量,计算可得.

【实验一】制取氯酸钾和氯水.
利用如图1所示实验装置和药品进行实验.
(1)装置A中玻璃仪器为圆底烧瓶和分液漏斗,若对调B和C装置的位置,可能(填“可能”或“不可能”)提高B中氯酸钾的产率.
【实验二】检验上述制备Cl2中混有的HCl.
选用图1装置A和图2所给装置以及药品进行实验.
(2)实验仪器接口连接顺序为:装置A→e、d→b、c→f、g→a.
能证明HCl存在的现象是④中淀粉-KI试纸不变蓝色,装置①中产生白色沉淀.
【实验三】氯酸钾与碘化钾反应的研究.
在不同条件下KClO3可将KI氧化为I2或KIO3.该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.20mol•L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol•L-1H2SO4/ml | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
【实验四】比较HClO与HCO3-电离常数的大小和测定饱和氯水中氯元素的总量.
查阅资料知:
i.实验室难以获得纯HClO溶液;
ii.次氯酸会破坏酸碱指示剂;
iii.次氯酸或氯气可被SO2、H2O2、和FeCl2等物质还原成Cl-.
(4)设计实验证明(实验方案不必描述操作过程的细节);
①相同条件下,HClO的电离常数大于HCO3-:配制相同物质的量浓度的碳酸钠和次氯酸钠溶液,用pH计分别测定两种溶液的pH值.
②确定饱和氯水中氯元素的总量:量取一定量的试样,加入足量的双氧水溶液,充分反应后,加热除去过量的双氧水,冷却,再加入足量的硝酸银溶液,过滤,洗净烘干后称量沉淀质量,计算可得.
17.基准物质邻苯二甲酸氢钾(KHC8H4O4)可用于标定( )
| A. | 酸 | B. | 碱 | C. | 还原剂 | D. | 氧化剂 |
7.丁烷催化裂化时碳碳键按两种方式断裂,生成两种烷烃和两种烯烃.如果丁烷的裂化率为60%,且裂化生成的两种烯烃物质的量相等,则裂化后得到的含氢质量分数最高的气体占混合气体的体积分数为( )
| A. | 18.75% | B. | 30% | C. | 15% | D. | 22.5% |
14.有4g铁的氧化物,用足量的CO在高温下将其还原,把生成的CO2全部通入足量澄清石灰水中,得到7.5g沉淀.这种铁的氧化物的化学式是( )
| A. | FeO | B. | Fe2O3 | C. | Fe3O4 | D. | FeO和Fe2O3 |
14.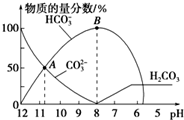 常温下,在10mL0.1mol•L-1Na2CO3溶液中逐渐加入0.1mol•L-1的盐酸,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数的变化如图所示(CO2因逸出未画出,忽略气体逸出而引起的溶液体积变化),下列说法正确的是( )
常温下,在10mL0.1mol•L-1Na2CO3溶液中逐渐加入0.1mol•L-1的盐酸,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数的变化如图所示(CO2因逸出未画出,忽略气体逸出而引起的溶液体积变化),下列说法正确的是( )
 常温下,在10mL0.1mol•L-1Na2CO3溶液中逐渐加入0.1mol•L-1的盐酸,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数的变化如图所示(CO2因逸出未画出,忽略气体逸出而引起的溶液体积变化),下列说法正确的是( )
常温下,在10mL0.1mol•L-1Na2CO3溶液中逐渐加入0.1mol•L-1的盐酸,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数的变化如图所示(CO2因逸出未画出,忽略气体逸出而引起的溶液体积变化),下列说法正确的是( )| A. | 在A点所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) | |
| B. | 在B点所示的溶液中,浓度最大的离子是HCO3- | |
| C. | 当溶液的pH为7时,溶液中的阴离子只有两种 | |
| D. | 25℃时,HCO3-的电离平衡常数Ka=5×10-11,当溶液的pH=10时,c(HCO3-)=2c(CO32-) |
15.已知:Fe2O3(s)+$\frac{3}{2}$C(s)═$\frac{3}{2}$CO2(g)+2Fe(s)△H=+234.1kJ•mol-1
C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
则2Fe(s)+O2(g)═Fe2O3(s)的△H是( )
C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
则2Fe(s)+O2(g)═Fe2O3(s)的△H是( )
| A. | -824.4kJ•mol-1 | B. | -627.6kJ•mol-1 | C. | -744.7kJ•mol-1 | D. | -169.4kJ•mol-1 |