题目内容
1.燃料电池是一种新能源.利用2CO+O 2 ═2CO 2 设计燃料电池时,负极发生反应的气体是CO,正极发生反应的气体是O2.分析 该燃料电池中,通入CO的一极为原电池的负极,发生氧化反应,通入氧气一极为原电池的正极,发生还原反应.
解答 解:由2CO+O2 ═2CO2 ,该燃料电池中通入CO的一极是负极,发生氧化反应,通O2的一极是正极,发生还原反应,故答案为:CO;O2.
点评 本题考查原电池原理,根据燃料电池的工作原理规律来分析解答即可,比较简单.

练习册系列答案
相关题目
11.关于氧化剂的叙述正确的是( )
| A. | 得电子越多,其氧化性越强 | B. | 分子中一定含有氧元素 | ||
| C. | 在反应中易失电子的物质 | D. | 在反应中易结合电子的物质 |
12.在一定条件下发生如下反应:COCl2(g)$\stackrel{催化剂}{?}$CO(g)+Cl2(g)△H<0下列有关说法正确的是( )
| A. | 单位时间内生成CO和Cl2的物质的量比为1:1时,反应达到平衡状态 | |
| B. | 用催化剂能提高反应物的平衡转化率 | |
| C. | 平衡时其他条件不变,升高温度能提高COCl2的转化率 | |
| D. | 当反应达平衡时,恒温恒压条件下通入Ar能提高COCl2的转化率 |
9.用NA表示阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 在标况下,22.4LSO3和22.4LC2H4原子个数比为2:3 | |
| B. | 将78gNa2O2与过量CO2反应转移的电子数为2NA | |
| C. | 28g乙烯分子中含有极性共价键的数目为6NA | |
| D. | 1molNaCl晶体中含有NA个Na+ |
16.几种相邻主族短周期元素的相对位置如表,元素X的原子核外电子数是M的2倍,Y的氧化物具有两性.下列说法不正确的是( )
| M | N | ||
| X | Y |
| A. | 元素的第一电离能X<Y | |
| B. | X位于第三周期 IIA,其单质可采用电解熔融其氯代物制备 | |
| C. | 元素最高价氧化物的水化物中,酸性最强的是HNO3 | |
| D. | 气体分子(MN)2的电子式为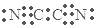 |
10.实验室需要用500mL 1.0mol/L Na2CO3溶液进行相关实验,下列有关配制该溶液的说法不正确的是( )
| A. | 用托盘天平称取53.0g Na2CO3固体 | |
| B. | 需要的玻璃仪器有500mL容量瓶、烧杯、玻璃棒、胶头滴管、量筒 | |
| C. | 转移溶液时有少量液体溅出,则最终溶液的浓度偏高 | |
| D. | 定容时仰视刻度线,则最终溶液的浓度偏低 |
12.下列应用涉及氧化还原反应的是( )
| A. | 人工固氮 | B. | 粗盐提纯 | C. | 工业制氧 | D. | 玻璃刻字 |
 .
.