题目内容
5.在一次学生实验中,学生用铝片分别和稀盐酸、稀硫酸反应,发现:铝片与稀盐酸反应现象非常明显,而与稀硫酸几乎不反应.这和教材中“铝能跟稀盐酸或稀硫酸反应生成氢气“的说法不一致.为排除因试剂变质等因素造成的影响,该学生在教师的指导下重新进行下列实验,验证是否存在上述现象.实验用品:仪器(略,凡是实验需要的均有提供)
药品:3.0mol/L盐酸、1.5mol/L硫酸、3.0mol/L硫酸,相同大小的铝片(纯度>99.5%)
实验过程:往三支相同的试管中分别加入相同的铝片各一片,再往试管中分别加入等体积的3.0mol/L盐酸、1.5mol/L硫酸、3.0mol/L硫酸,观察反应进行到1、2、5、15、20分钟时的铝与酸反应的情况.结果如下:
| 反应进程(分钟) | 1 | 2 | 5 | 15 | 20 | |
| 实验1 | 3.0mol/L盐酸 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
| 实验2 | 1.5mol/L硫酸 | 均无明显现象(无气泡产生) | ||||
| 实验3 | 3.0mol/L硫酸 | 均无明显现象(无气泡产生) | ||||
(1)写出铝与盐酸反应的离子方程式是2Al+6H+═2Al3++3H2↑
(2)反应1~15min内,铝与盐酸的反应速率逐渐加快,其原因是反应放出热量,温度升高,使化学反应速率加快.
(3)将实验2中硫酸的浓度设计为1.5mol/L的依据是统一氢离子的浓度,比较阴离子在反应中的不同作用
(4)根据以上探究“铝与稀盐酸和稀硫酸反应差异的原因”,你能对问题原因作出哪些假设或猜想(列出两种即可)?
假设一:促进金属铝表面的氧化膜与H+反应
假设二:对金属铝表面的氧化膜与H+反应起阻碍作用.
分析 (1)铝能置换出酸中的氢;
(2)温度越高反应速率越快,金属和酸的反应是放热反应;
(3)1.5mol/L的硫酸中氢离子浓度与3mol/L的盐酸中氢离子浓度相同,铝与酸反应的实质是铝与氢离子的反应,从而得出硫酸根与氯离子在反应中起到不同的作用;
(4)利用固定变量法探究氯离子和硫酸根离子对金属铝表面的氧化膜与H+反应的影响.
解答 解:(1)铝能置换出酸中氢离子,离子方程式为:2Al+6H+═2Al3++3H2↑,
故答案为:2Al+6H+═2Al3++3H2↑;
(2)反应1~15min内,铝与酸的反应是放出热量的,导致温度升高,使化学反应速率加快,
故答案为:反应放出热量,温度升高,使化学反应速率加快;
(3)1.5mol/L的硫酸中氢离子浓度与3mol/L的盐酸中氢离子浓度相同,铝与酸反应的实质是铝与氢离子的反应,在反应的条件中,只有阴离子不同,从反应现象得出硫酸根与氯离子在反应中起到不同的作用,将实验2中硫酸的浓度设计为1.5mol/L的依据是统一氢离子的浓度,比较阴离子在反应中的不同作用,
故答案为:统一氢离子的浓度,比较阴离子在反应中的不同作用;
(4)在铝的表面有一层致密氧化铝薄膜,当加入盐酸和硫酸溶时,酸液首先与氧化铝薄膜反应,由反应的现象可知,铝片和稀盐酸反应现象明显,而和稀硫酸几乎不反应,比较盐酸和硫酸溶液中含有的离子的不同,出现这种现象的原因可能是:氯离子促进金属铝表面的氧化膜与H+反应,硫酸根离子对金属铝表面的氧化膜与H+反应对起阻碍作用,所以假设一:促进金属铝表面的氧化膜与H+反应;假设二:对金属铝表面的氧化膜与H+反应起阻碍作用,
故答案为:促进金属铝表面的氧化膜与H+反应;对金属铝表面的氧化膜与H+反应起阻碍作用.
点评 本题探究影响化学反应速率的因素,考查除浓度、温度等常考条件外的其他条件,题目新颖,特别注意利用控制变量法设计实验论证假设.

| A. | 用AgNO3溶液可以鉴别KCl和KI | |
| B. | SO2使溴水褪色与乙烯使KMnO4溶液褪色原理相同 | |
| C. | 可根据硫酸密度的大小判断铅蓄电池是否需要充电 | |
| D. | 制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸 |
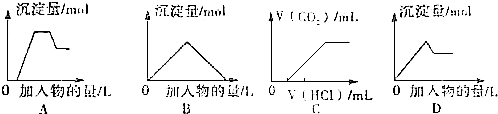
| A. | 图A表示想含OH-、AlO2-、CO32-、SiO32-、的溶液中滴加HCL溶液产生沉淀量的关系曲线 | |
| B. | 图B表示向澄清石灰水中通入二氧化碳直至过量产生沉淀量的关系曲线 | |
| C. | 图C表示向NaOH和Na2CO3的混合液中滴加盐酸产生CO2气体的关系曲线 | |
| D. | 图D表示向明矾溶液中滴加Ba(OH)2溶液产生沉淀量的关系曲线 |
| A. | ③⑥①②⑤④ | B. | ⑤①②⑥④③ | C. | ⑤④③②①⑥ | D. | ③①②④⑤⑥ |
 某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,在实验室中用标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:
某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,在实验室中用标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:| 指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
| 变色范围(pH) | 5.0~8.0 | 3.1~4.4 | 4.4~6.2 | 8.2~10.0 |
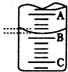
(2)如图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为25.40mL.
(3)为了减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准液浓度为c mo1/L,三次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.35 | 25.30 |
A.实验结束时俯视滴定管中液面,读取滴定终点时NaOH溶液的体积
B.滴加NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
C.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗,
(4)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式:C=$\frac{c×(25.35+25.30)}{2V}$.
 有机物之间的反应通常比较复杂,同样的反应物在不同条件下生成不同的产物.
有机物之间的反应通常比较复杂,同样的反应物在不同条件下生成不同的产物.