题目内容
K2Cr2O7(橙色)、Cr2(SO4)3(绿色)、K2SO4、H2SO4、C2H5OH、CH3COOH和H2O分别属于同一氧化还原反应中的反应物和生成物,该反应原理可以用于检查司机是否酒后开车.
(1)该反应中的还原剂是 .
(2)若司机酒后开车,检测仪器内物质显示出 色.
(3)在反应中,铬元素的化合价从 价变为 价.
(4)写出并配平该反应的化学方程式 .
(5)如果在反应中生成1mol氧化产物,转移的电子总数为 .
(1)该反应中的还原剂是
(2)若司机酒后开车,检测仪器内物质显示出
(3)在反应中,铬元素的化合价从
(4)写出并配平该反应的化学方程式
(5)如果在反应中生成1mol氧化产物,转移的电子总数为
考点:氧化还原反应
专题:氧化还原反应专题
分析:该反应原理可以用于检查司机是否酒后开车,乙醇是反应物,乙醇反应生成乙酸,碳元素失电子化合价升高,所以乙醇作还原剂;要使反应发生氧化还原反应,必须元素有化合价升高的和化合价降低的才可,乙醇作还原剂,必须有另一种物质得电子化合价降低,K2Cr2O7(橙色)中铬元素的化合价是+6价,Cr2(SO4)3(绿色)中化合价为+3价,所以K2Cr2O7(橙色)作氧化剂,还原产物是Cr2(SO4)3(绿色),所以K2Cr2O7、C2H5OH为反应物,Cr2(SO4)3、CH3COOH为生成物,根据元素守恒得,硫酸为反应物,硫酸钾、水为生成物,然后根据得失电子数相等配平,所以反应方程式为2K2Cr2O7+3C2H5OH+8H2SO4=2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O,以此来解答.
解答:
解:(1)反应原理可以用于检查司机是否酒后开车,乙醇是反应物,乙醇反应生成乙酸,碳元素失电子化合价升高,所以乙醇作还原剂,故答案为:C2H5OH;
(2)C元素的化合价升高,则Cr元素的化合价降低,发生K2Cr2O7(橙色)→Cr2(SO4)3(绿色),则检测仪器内物质显示出绿色,故答案为:绿;
(3)由上述分析可知,发生K2Cr2O7(橙色)→Cr2(SO4)3(绿色),则Cr元素的化合价由+6价变为+3价,故答案为:+6;+3;
(4)K2Cr2O7、C2H5OH为反应物,Cr2(SO4)3、CH3COOH为生成物,根据元素守恒得,硫酸为反应物,硫酸钾、水为生成物,然后根据得失电子数相等配平,所以反应方程式为2K2Cr2O7+3C2H5OH+8H2SO4=2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O,
故答案为:2K2Cr2O7+3C2H5OH+8H2SO4=2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O;
(5)乙醇被氧化为乙酸,则乙酸为氧化产物,生成1mol氧化产物,由C元素的化合价变化可知转移的电子总数为1mol×2×(2-0)×NA=2.408×1024或4NA,
故答案为:2.408×1024或4NA.
(2)C元素的化合价升高,则Cr元素的化合价降低,发生K2Cr2O7(橙色)→Cr2(SO4)3(绿色),则检测仪器内物质显示出绿色,故答案为:绿;
(3)由上述分析可知,发生K2Cr2O7(橙色)→Cr2(SO4)3(绿色),则Cr元素的化合价由+6价变为+3价,故答案为:+6;+3;
(4)K2Cr2O7、C2H5OH为反应物,Cr2(SO4)3、CH3COOH为生成物,根据元素守恒得,硫酸为反应物,硫酸钾、水为生成物,然后根据得失电子数相等配平,所以反应方程式为2K2Cr2O7+3C2H5OH+8H2SO4=2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O,
故答案为:2K2Cr2O7+3C2H5OH+8H2SO4=2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O;
(5)乙醇被氧化为乙酸,则乙酸为氧化产物,生成1mol氧化产物,由C元素的化合价变化可知转移的电子总数为1mol×2×(2-0)×NA=2.408×1024或4NA,
故答案为:2.408×1024或4NA.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析能力和氧化还原反应基本概念、转移电子的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知一些物质的标准燃烧热:
等质量的下列物质充分燃烧放出热量最多的是( )
| 燃料 | H2 | CH4 | C2H2 | C2H5OH |
| 燃烧热△H/KJ.mol-1 | -285.8 | -890.3 | -1299.6 | -1366.8 |
| A、H2 |
| B、CH4 |
| C、C2H2 |
| D、C2H5OH |

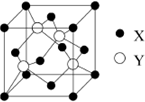 元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p 轨道上有4个电子.元素Z 的原子最外层电子数是其内层的3倍.
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p 轨道上有4个电子.元素Z 的原子最外层电子数是其内层的3倍.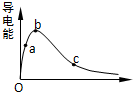 一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,
一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,
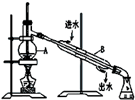
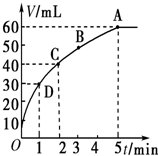 l mol MnO2粉末加入50mL过氧化氢的溶液里(ρ=1.1g?L-1),在标准状况下,放出气体的体积y和时间t的关系曲线如图所示.
l mol MnO2粉末加入50mL过氧化氢的溶液里(ρ=1.1g?L-1),在标准状况下,放出气体的体积y和时间t的关系曲线如图所示. 如图所示转化关系,已知A为气体单质,判断A是什么物质,并写出有关的化学方程式.
如图所示转化关系,已知A为气体单质,判断A是什么物质,并写出有关的化学方程式.