题目内容
下列化学事实及其结论都正确的是( )
| A、铝制饮具最好不要盛放酸性、或碱性较强的液体食物,因为Al和Al2O3既可以与酸反应、又可以与碱反应 |
| B、将SO2通入含HClO的溶液中,生成H2SO4,说明HClO酸性比H2SO4 强 |
| C、FeCl3溶液可以腐蚀线路板上的Cu,说明Fe的金属活动性大于Cu |
| D、过量的铜屑与稀硝酸作用,反应停止后,再加入1mol/L稀硫酸,铜屑又逐渐溶解是因为铜可直接与1mol/L稀硫酸反应 |
考点:铝的化学性质,二氧化硫的化学性质,铁的氧化物和氢氧化物,铜金属及其重要化合物的主要性质
专题:元素及其化合物
分析:A.二者有因果关系;
B.二氧化硫具有还原性,次氯酸具有强氧化性;
C.三价铁的氧化性大于铜离子;
D.铜屑与稀硝酸能反应,但铜和稀硫酸不反应.
B.二氧化硫具有还原性,次氯酸具有强氧化性;
C.三价铁的氧化性大于铜离子;
D.铜屑与稀硝酸能反应,但铜和稀硫酸不反应.
解答:
解:A.因为Al和Al2O3既可以与酸反应,又可以与碱反应,则不要盛放酸性或碱性较强的液体食物,二者有因果关系,故A正确;
B.二氧化硫具有还原性,次氯酸具有强氧化性,生成H2SO4发生了氧化还原反应,故B错误;
C.FeCl3溶液可以腐蚀线路板上的Cu,说明三价铁的氧化性大于铜离子,故C错误;
D.铜屑与稀硝酸反应方程式为:3Cu+8 HNO3=3Cu(NO3)2 +2 NO↑+4H2O,离子反应方程式为3Cu+8 H++2 NO3-=Cu2++2 NO↑+4H2O,当过量的铜屑与稀硝酸作用,反应停止后,从离子反应方程式可看出H+全部消耗,但NO3-剩余,再加入1mol/L稀硫酸,相当于又加入H+,仍发生铜屑与稀硝酸的反应,铜与稀硫酸不反应,故D错误.
故选A.
B.二氧化硫具有还原性,次氯酸具有强氧化性,生成H2SO4发生了氧化还原反应,故B错误;
C.FeCl3溶液可以腐蚀线路板上的Cu,说明三价铁的氧化性大于铜离子,故C错误;
D.铜屑与稀硝酸反应方程式为:3Cu+8 HNO3=3Cu(NO3)2 +2 NO↑+4H2O,离子反应方程式为3Cu+8 H++2 NO3-=Cu2++2 NO↑+4H2O,当过量的铜屑与稀硝酸作用,反应停止后,从离子反应方程式可看出H+全部消耗,但NO3-剩余,再加入1mol/L稀硫酸,相当于又加入H+,仍发生铜屑与稀硝酸的反应,铜与稀硫酸不反应,故D错误.
故选A.
点评:本题考查化学实验方案的评价,为高考常见题型,侧重于学生的实验能力和评价能力的考查,明确物质的性质为解答该题的关键,难度不大.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
化学与人类生活密切相关.下列说法中不正确的是( )
| A、伦敦奥运会中采用的新型氢动力计程车可以降低PM2.5的排放,减小大气污染 |
| B、酸雨就是pH<7的雨水,主要是由大气中的SO2、NO2等造成的 |
| C、绚丽缤纷的烟花中添加了含钾、钠、钙、铜等金属元素的化合物 |
| D、服用铬含量超标的药用胶囊会对人体健康造成危害 |
碱性电池具有容量大、放电电流大的特点,因而得到广泛使用,锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应为:Zn(s)+2MnO2(s)+H2O(l)﹦Zn(OH)2(s)+Mn2O3(s)下列说法错误的是( )
| A、电池工作时,锌失去电子 |
| B、反应时化学能转化为电能 |
| C、电池工作时,电子由正极通过外电路流向负极 |
| D、外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
维胺酯(Viaminati),治疗各种痤疮、角化异常性皮肤病,结构如图.下列有关维胺酯说法不正确的是( )
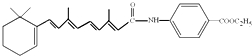

| A、不溶于水,服用后在胃酸作用下能水解 |
| B、在氢氧化钠溶液中水解,1mol维胺酯最多消耗氢氧化钠2mol |
| C、能发生加聚、加成、酯化等反应 |
| D、一定条件下,与溴的四氯化碳反应,1mol维胺酯最多消耗溴5mol |
下列离子方程式中,正确的是( )
| A、稀硫酸滴在铁片上:2Fe+6H+=2Fe3++3H2↑ |
| B、NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO32-+H2O |
| C、硫酸铜溶液与氢氧化钠溶液混合:CuS04+20H-=Cu(OH)2↓+SO42- |
| D、硝酸银溶液与氯化钠溶液混合:AgNO3+Cl-=AgCl↓+NO3- |
下列有关胶体的说法正确的是( )
| A、胶体都是澄清透明的 |
| B、胶体与溶液的本质区别是有丁达尔效应 |
| C、将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可得氢氧化铁胶体 |
| D、胶体一定是混合物 |