题目内容
17.下列溶液中各微粒的浓度关系不正确的是( )| A. | pH=2的HA溶液与pH=12的MOH溶液任意比混合:c(H+)+c(M+)═c(OH-)+c(A-) | |
| B. | 1 L 0.1 mol•L-1 (NH4)2Fe(SO4)2的溶液中:c(SO${\;}_{4}^{2-}$)>c(NH${\;}_{4}^{+}$)>c(Fe2+)>c(H+)>c(OH-) | |
| C. | 0.1 mol•L-1 NaHCO3溶液中:c(H+)+c(H2CO3)═c(CO${\;}_{3}^{2-}$)+c(OH-) | |
| D. | 0.1mol•L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
分析 A.根据溶液的电荷守恒进行判断;
B.硫酸根离子不水解,而铵根离子水解,铵根离子与亚铁离子水解溶液呈酸性;
C.根据质子守恒进行判断;
D.0.1 mol/L的NaHA溶液,其pH=4,说明HA-电离程度大于水解程度.
解答 解:A.pH=2的HA溶液与pH=12的MOH溶液以任意比混合,溶液都不显电性,由电荷守恒可知,c(H+)+c(M+)=c(OH-)+c(A-),故A正确;
B.硫酸根离子不水解,而铵根离子水解,铵根离子与亚铁离子水解溶液呈酸性,所以离子浓度的大小为:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-),故B正确;
C.0.1 mol•L-1 NaHCO3溶液中,根据质子守恒可知:c(H+)+c(H2CO3)═c(CO32-)+c(OH-),故C正确;
D.pH=4,则HA-的电离大于其水解,电离生成A2-,则c(HA-)>c(H+)>c(A2-)>c(H2A),故D错误.
故选D.
点评 本题考查离子浓度大小的比较,明确盐类水解、电离、浓度与pH 的关系及物料守恒、电荷守恒即可解答,难度较大.

练习册系列答案
相关题目
7.A、B、C、D、E、F是元素周期表前四周期中原子序数依次增大的六种常见元素,其相关信息如表:
回答下列问题:
(1)元素E在元素周期表中的位于第四周期第Ⅷ族,其高价态离子核外有5个未成对电子
(2)B、C、D三种元素的离子半径由小到大的顺序是r(Al3+)<r(O2-)<r(C1-)(用离子符号表示).
(3)A、D两元素的简单氢化物发生反应生成的化合物的电子式为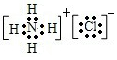
(4)常温下AD3是一种淡黄色液体.以下关于AD3的说法中,正确的是BC
A.AD3分子中只有非极性键 B.AD3分子中各原子均达8e-稳定结构
C.AD3的晶体属于分子晶体 D.AD3液体气化时化学键被破坏
(5)金属C与E的黑色磁性晶体氧化物在高温下反应,该反应的化学方程式为3Fe3O4+8Al$\frac{\underline{\;高温\;}}{\;}$9Fe+4Al2O3
(6)向F的硫酸盐溶液中通入AH3气体至过量,观察到的现象是蓝色溶液先产生蓝色沉淀,最后沉淀溶解,形成深蓝色溶液;该过程总的离子反应式为Cu2++4NH3=[Cu(NH3)4]2+或Cu2++4 NH3•H2O=[Cu(NH3)4]2++4H2O向反应后的溶液中加入适量乙醇,析出深蓝色晶体,该晶体中不含有的化学键类型是C
A.配位键 B.极性共价键 C.非极性共价键 D.离子键.
| 元素 | 相 关 信 息 |
| A | 原子核外有7种运动状态不同的电子 |
| B | 外围电子排布式为nsnnpn+2 |
| C | 常见的金属,在周期表中周期序数与族序数相等 |
| D | 气态氢化物及最高价氧化物对应的水化物均为强酸 |
| E | 一种核素的质量数为56,中子数为30 |
| F | 单质紫红色,电缆材料,常见氧化物为黑色 |
(1)元素E在元素周期表中的位于第四周期第Ⅷ族,其高价态离子核外有5个未成对电子
(2)B、C、D三种元素的离子半径由小到大的顺序是r(Al3+)<r(O2-)<r(C1-)(用离子符号表示).
(3)A、D两元素的简单氢化物发生反应生成的化合物的电子式为
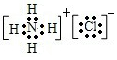
(4)常温下AD3是一种淡黄色液体.以下关于AD3的说法中,正确的是BC
A.AD3分子中只有非极性键 B.AD3分子中各原子均达8e-稳定结构
C.AD3的晶体属于分子晶体 D.AD3液体气化时化学键被破坏
(5)金属C与E的黑色磁性晶体氧化物在高温下反应,该反应的化学方程式为3Fe3O4+8Al$\frac{\underline{\;高温\;}}{\;}$9Fe+4Al2O3
(6)向F的硫酸盐溶液中通入AH3气体至过量,观察到的现象是蓝色溶液先产生蓝色沉淀,最后沉淀溶解,形成深蓝色溶液;该过程总的离子反应式为Cu2++4NH3=[Cu(NH3)4]2+或Cu2++4 NH3•H2O=[Cu(NH3)4]2++4H2O向反应后的溶液中加入适量乙醇,析出深蓝色晶体,该晶体中不含有的化学键类型是C
A.配位键 B.极性共价键 C.非极性共价键 D.离子键.
8.西瓜膨大剂别名氯吡苯脲,是经过国家批准的植物生长调节剂,实践证明长期使用对人体无害.已知其相关性质如表所示:
(1)氯元素基态原子核外电子的成对电子数为16,氯吡苯脲中所含元素能形成10电子分子,且分子之间能形成氢键的有NH3、H2O.(填二种,填化学式)
(2)氯吡苯脲的晶体类型为分子晶体.该分子是由极性、非极性键形成的极性分子(填“极性”或“非极性”)
| 分子式 | 结构简式 | 外观 | 熔点 | 溶解性 |
| C12H10ClN3O | 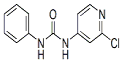 | 白色结晶粉末 | 170~172°C | 易溶于水 |
(2)氯吡苯脲的晶体类型为分子晶体.该分子是由极性、非极性键形成的极性分子(填“极性”或“非极性”)
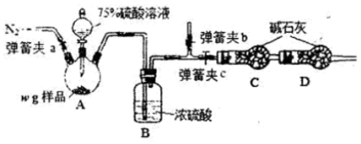
5.用下列装置完成相关实验,合理的是( )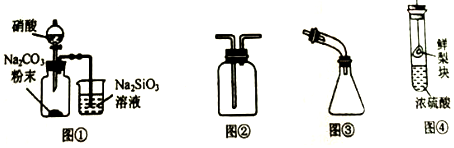

| A. | 图①:证明非金属性由强到弱的顺序是N>C>Si | |
| B. | 图②:收集NO2或NH3 | |
| C. | 图③:海水蒸馏时接收蒸馏水 | |
| D. | 图④:探究浓硫酸的脱水性 |
2.某固体化合物的化学式NH5,它的所有原子的最外层都符合稀有气体原子的电子层结构,则下列说法中,正确的是( )
| A. | 它与足量的水反应的化学方程式为:NH5+H2O═NH3•H2O+H2↑ | |
| B. | NH5中只有极性共价键的共价化合物 | |
| C. | 1molNH5中含有5NA个N-H键(NA表示阿伏伽德罗常数) | |
| D. | NH5中所有原子最外层均为8个电子 |
5. (1)溶液的pH除了可以通过实验得出的具体数据计算得到,在实验室中还可以用pH试纸或pH计来测量得到.
(1)溶液的pH除了可以通过实验得出的具体数据计算得到,在实验室中还可以用pH试纸或pH计来测量得到.
(2)某研究性学习小组用pH=1的盐酸滴定25.00mL未知物质的量浓度的NaOH溶液,从而求出该NaOH溶液的pH值(选用酚酞作为指示剂)
①实验过程中需要使用的仪器有铁架台、滴定管夹、碱式滴定管、胶头滴管、酸式滴定管、锥形瓶
②如图,是某次滴定时的滴定管中的液面,其读数为22.60mL;
③如何判断滴定到达终点当滴加最后一滴盐酸,溶液的颜色由黄色变为橙色,且在半分钟内不变色
④根据下列数据:
请计算待测NaOH溶液的浓度(保留两位小数)0.0800 mol/L
⑤在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有:BD.
A.滴定终点读数时俯视读数
B.酸式滴定管使用前,水洗后未用盐酸溶液润洗
C.锥形瓶水洗后未干燥
D.酸式滴定管尖嘴部分有气泡,滴定后消失.
 (1)溶液的pH除了可以通过实验得出的具体数据计算得到,在实验室中还可以用pH试纸或pH计来测量得到.
(1)溶液的pH除了可以通过实验得出的具体数据计算得到,在实验室中还可以用pH试纸或pH计来测量得到.(2)某研究性学习小组用pH=1的盐酸滴定25.00mL未知物质的量浓度的NaOH溶液,从而求出该NaOH溶液的pH值(选用酚酞作为指示剂)
①实验过程中需要使用的仪器有铁架台、滴定管夹、碱式滴定管、胶头滴管、酸式滴定管、锥形瓶
②如图,是某次滴定时的滴定管中的液面,其读数为22.60mL;
③如何判断滴定到达终点当滴加最后一滴盐酸,溶液的颜色由黄色变为橙色,且在半分钟内不变色
④根据下列数据:
| 滴定次数 | 待测液体积(mL)[来源 | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 4.00 | 24.10 |
⑤在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有:BD.
A.滴定终点读数时俯视读数
B.酸式滴定管使用前,水洗后未用盐酸溶液润洗
C.锥形瓶水洗后未干燥
D.酸式滴定管尖嘴部分有气泡,滴定后消失.
6.下列关于苯的叙述正确的是( )
| A. | 不能和氢气反应 | B. | 属于不饱和烃 | ||
| C. | 能使酸性高锰酸钾溶液褪色 | D. | 含有碳碳双键 |
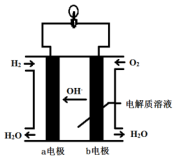 英国一家公司正在研发全球首款“充一次电,用七天”的碱性氢氧燃料手机电池.如图为碱性氢氧燃料电池结构示意图.
英国一家公司正在研发全球首款“充一次电,用七天”的碱性氢氧燃料手机电池.如图为碱性氢氧燃料电池结构示意图.