题目内容
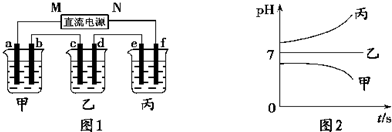
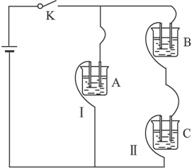
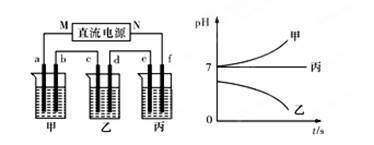
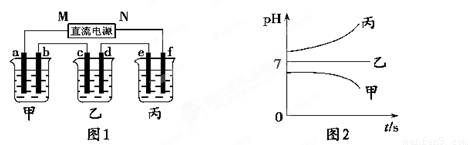
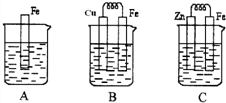 如图A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸.
如图A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸.(1)A中反应的离子方程式是
Fe+2H+=Fe2++H2↑
Fe+2H+=Fe2++H2↑
.(2)B中Cu极的电极反应式是
2H++2e_=H2↑;
2H++2e_=H2↑;
.Cu极附近溶液的pH
增大
增大
(填“增大”、“减小”或“不变”).(3)C中被腐蚀的金属是
Zn
Zn
(填化学式),A、B、C中铁被腐蚀的速率,由快到慢的顺序是B>A>C
B>A>C
(用“>”表示).分析:(1)根据离子方程式的书写规则书写;
(2)先判断正负极,再判断铜极上的反应类型,从而写出电极反应式;根据氢离子的浓度变化判断;
(3)根据电极的正负极判断;根据所作电极判断;
(2)先判断正负极,再判断铜极上的反应类型,从而写出电极反应式;根据氢离子的浓度变化判断;
(3)根据电极的正负极判断;根据所作电极判断;
解答:解:(1)硫酸、硫酸亚铁是可溶性的强电解质,写离子,铁、氢气是单质写化学式,铁和稀硫酸反应生成硫酸亚铁和氢气.
故答案为:Fe+2H+=Fe2++H2↑
(2)B中Cu作正极,氢离子在铜极上得电子生成氢气,反应还原反应;氢离子在铜极上生成氢气,使溶液中的氢离子浓度降低,所以PH增大.
故答案为:2H++2e_=H2↑; 增大.
(3)C中锌作负极,锌失电子变成离子进入溶液,所以被腐蚀的是锌;A中铁和稀硫酸反应;B中铁作负极,加快铁的腐蚀;C中铁作正极,减慢铁的腐蚀.
故答案为:Zn; B>A>C
故答案为:Fe+2H+=Fe2++H2↑
(2)B中Cu作正极,氢离子在铜极上得电子生成氢气,反应还原反应;氢离子在铜极上生成氢气,使溶液中的氢离子浓度降低,所以PH增大.
故答案为:2H++2e_=H2↑; 增大.
(3)C中锌作负极,锌失电子变成离子进入溶液,所以被腐蚀的是锌;A中铁和稀硫酸反应;B中铁作负极,加快铁的腐蚀;C中铁作正极,减慢铁的腐蚀.
故答案为:Zn; B>A>C
点评:不同条件下金属腐蚀的快慢规律:
电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀
电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀

练习册系列答案
相关题目