题目内容
9.某有机物Z具有较广泛的抗菌作用,其生成机理可由X与Y相互作用.下列有关叙述中不正确的是( )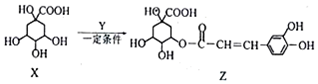
| A. | X能使酸性高锰酸钾溶液褪色 | |
| B. | Y的分子式为C9H8O3 | |
| C. | 1mol Z与足量NaOH溶液反应,最多消耗8mol NaOH | |
| D. | Z与浓溴水既能发生取代反应又能发生加成反应 |
分析 A.X含有羟基,可被高锰酸钾氧化;
B.由酯化反应及原子守恒可知Y的分子式;
C.Z中-COOH、-COOC-、酚-OH均与NaOH;
D.Z中含酚-OH、碳碳双键.
解答 解:A.X含有羟基,可被高锰酸钾氧化,能使酸性高锰酸钾溶液褪色,故A正确;
B.由结构简式X为C7H12O6,Z分子式为C16H18O9,由酯化反应规律可知Y的分子式为C9H8O4,故B错误;
C.Z中-COOH、-COOC-、酚-OH均与NaOH,则1mol Z与足量NaOH溶液反应,最多消耗4mol NaOH,故C错误;
D.Z中含酚-OH、碳碳双键,酚-OH的邻对位与溴水发生取代反应,碳碳双键与溴水发生加成,故D正确;
故选BC.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、酯性质的考查,选项B为易错点,题目难度不大.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
19.设NA表示阿伏伽德罗常数的值,下列说法不正确的是( )
| A. | 4.0g 氦气中含有的最外层电子数为4NA | |
| B. | 3.9g 2H37Cl中含有的中子数为2.1NA | |
| C. | 标准状况下,11.2L丙烷中含有的非极性键数目为NA | |
| D. | 100mL 1mol•L-1 CH3COOH溶液中含有的分子数目大于0.1NA |
20.工业上可由乙苯生产苯乙烯,反应原理如下: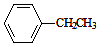 $→_{加热}^{Fe_{2}O_{3}}$
$→_{加热}^{Fe_{2}O_{3}}$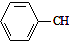 =CH2+H2,下列说法正确的是( )
=CH2+H2,下列说法正确的是( )
 $→_{加热}^{Fe_{2}O_{3}}$
$→_{加热}^{Fe_{2}O_{3}}$ =CH2+H2,下列说法正确的是( )
=CH2+H2,下列说法正确的是( )| A. | 酸性高锰酸钾溶液和溴水都可以用来鉴别乙苯和苯乙烯 | |
| B. | 乙苯、苯乙烯均能发生取代反应、加聚反应,氧化反应 | |
| C. | 乙苯的一氯取代产物有共有5种 | |
| D. | 乙苯和苯乙烯分子内共平面的碳原子数最多均为7 |
17.下列实验操作能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 配制SnCl2溶液 | 将SnCl2固体溶于适量的蒸馏水 |
| B | AlCl3溶液制备无水AlCl3 | 向AlCl3溶液中加入盐酸后直接蒸干 |
| C | 检验溶液中的SO42-离子 | 向溶液中加入盐酸酸化的氯化钡溶液 |
| D | 除去KNO3固体中少量的NaCl | 将固体溶解后蒸发浓缩,冷却结晶,过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
4.某溶液中只可能含有下列离子中的某几种:Na+、NH4+、Ba2+、SO42-、Br-、AlO2-.分别取样:①用pH计测试,溶液显弱酸性 ②加氯水和CCl4振荡后静置,下层呈无色,为确定该溶液的组成,还需检验的离子是( )
| A. | Na+ | B. | SO42- | C. | Ba2+ | D. | NH4+ |
5.为除去括号内的杂质,所选用的试剂或方法正确的是( )
| A. | Na2CO3溶液(Na2SO4),加入适量的Ba(OH)2溶液,过滤 | |
| B. | NaHCO3溶液(Na2CO3),通入过量的CO2气体 | |
| C. | 铝粉(Mg),加入足量的盐酸,过滤 | |
| D. | FeCl2溶液(FeCl3),通入足量的氯气 |
12.能用离子方程式“H++OH-═H2O”表示的化学反应是( )
| A. | 4HNO3$\frac{\underline{\;光照\;}}{\;}$2H2O+4H2O↑+O2↑ | B. | NaOH+HCl═NaCl+H2O | ||
| C. | CaCO3+2HCl═CaCl2+CO2↑+H2 | D. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O |
9.在一密闭容器中,CO和H2O混合加热到800℃达到下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g),K=1.0,若反应开始时CO和H2O的浓度分别为0.20mol/L和1.00mol/L,则CO转化为CO2的转化率为( )
| A. | 80% | B. | 83% | C. | 75% | D. | 91% |
10.在蒸发皿中蒸干下列物质的溶液,不能得到该物质固体的是( )
| A. | MgCl2 | B. | Fe2(SO4)3 | C. | K2CO3 | D. | NaCl |