题目内容
在8NH3+3Cl2═N2+6NH4Cl反应中,在该反应中氧化剂和还原剂的分子个数之比是( )
| A、3:1 | B、3:8 |
| C、3:2 | D、8:3 |
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:3Cl2+8NH3═6NH4Cl+N2中,Cl元素的化合价降低,N元素的化合价升高,化合价升高元素所在的反应物是还原剂,化合价降低元素所在的反应物是氧化剂.
解答:
解:3Cl2+8NH3═6NH4Cl+N2中,Cl元素的化合价降低,化合价降低元素所在的反应物是氧化剂,则氧化剂为Cl2,N元素的化合价升高,化合价升高元素所在的反应物是还原剂,还原剂是NH3,由反应可知3mol氧化剂氯气与2mol还原剂氨气反应电子守恒,则氧化剂与还原剂的物质的量之比=分子个数之比是=3:2,
故选C.
故选C.
点评:本题考查氧化还原反应,为高考常考考点,侧重基本概念的考查,明确反应中元素的化合价变化即可解答,题目难度不大.

练习册系列答案
相关题目
可逆反应N2+3H2?2NH3;△H<0.当单独改变下列条件后,有关叙述中错误的是( )
| A、体积不变,加入氩气,v正、v逆都增大,且v正增大倍数大于v逆增大倍数 |
| B、加入催化剂,v正、v逆都发生变化,且变化的倍数相同 |
| C、压缩体积,增大压强时,v正、v逆都增大,且v正增大倍数大于v逆增大倍数 |
| D、降低温度时,v正、v逆都减小,且v正减小倍数小于v逆减小倍数 |
下列反应中,不属于氧化还原反应的是( )
A、H2+Cl2
| ||||
B、2KMnO4
| ||||
| C、CaO+H2O=Ca(OH)2 | ||||
| D、Zn+H2SO4=ZnSO4+H2↑ |
浓硫酸滴到纸片上,纸片马上变黑,这是因为浓硫酸具有( )
| A、脱水性 | B、吸水性 |
| C、强酸性 | D、强氧化性 |
在一定条件下,在容积为2L的密闭容器中,将2mol气体M和3mol N气体混合,发生如下反应:2M(g)+3N(g)?x Q(g)+3R(g),该反应达平衡时,生成2.4mol R,并测得Q的浓度为0.4mol/L,下列有关叙述正确的是( )
| A、x值为2 |
| B、混合气体的密度增大 |
| C、平衡时N的浓度为0.3 mol/L |
| D、N的转化率为60% |
某种ABS工程树脂,由丙烯腈(CH2=CHCN,符号A)、1,3-丁二烯(CH2=CHCH=CH2,符号B)和苯乙烯(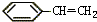 ,符号S)按一定配比共聚而得.经元素分析可知该ABS样品的组成为CaHbNc(a、b、c为正整数),则原料中A和B的物质的量之比用a、b、c表示是( )
,符号S)按一定配比共聚而得.经元素分析可知该ABS样品的组成为CaHbNc(a、b、c为正整数),则原料中A和B的物质的量之比用a、b、c表示是( )
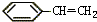 ,符号S)按一定配比共聚而得.经元素分析可知该ABS样品的组成为CaHbNc(a、b、c为正整数),则原料中A和B的物质的量之比用a、b、c表示是( )
,符号S)按一定配比共聚而得.经元素分析可知该ABS样品的组成为CaHbNc(a、b、c为正整数),则原料中A和B的物质的量之比用a、b、c表示是( )A、
| ||
B、
| ||
C、
| ||
| D、无法确定 |
实验室中需2mol/L的CuSO4溶液950ml,配制时应选用的容量瓶的规格和称取的CuSO4?5H2O的质量分别是( )
| A、1000ml,500g |
| B、950ml,475g |
| C、1000ml,490g |
| D、50 ml,304g |
抗酸药中既能与强酸反应,又能与强碱反应得物质是( )
| A、CaCO3 |
| B、Al(OH)3 |
| C、Mg(OH)2 |
| D、NaHCO3 |