题目内容
12.下列各组物质中,化学键类型不同的是( )| A. | NaCl和H2O2 | B. | H2O和NH3 | C. | CaF2和CsCl | D. | CCl4和HCl |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,第IA、第IIA族和第VIA、第VIIA族元素之间易形成离子键.
解答 解:A.NaCl中钠离子和氯离子之间只存在离子键,H2O2中H原子和O原子之间和O原子与O原子之间只存在共价键,所以两者化学键类型不同,故A正确;
B.水分子中H原子和O原子之间只存在形成共价键,氨气分子中N原子和H原子之间只存在共价键,故B错误;
C.氟化钙中氟离子和钙离子之间只存在离子键,氯化铯中铯离子和氯离子之间只存在离子键,故C错误;
D.四氯化碳中碳原子和氯原子之间只存在共价键、HCl中氯原子和氢原子之间只存在共价键,故D错误;
故选A.
点评 本题考查了化学键的判断,明确离子键和共价键的区别是解本题关键,易错选项是C,注意氟化钙中两个氟离子之间不存在共价键,为易错点.

练习册系列答案
相关题目
2.在一个盛有5mL澄清饱和石灰水的试管中,放入一小块金属钠,不可能观察到的现象是( )
| A. | 钠融化成银白色小球 | B. | 小球在液面上快速游动 | ||
| C. | 溶液底部出现银白色固体 | D. | 溶液变浑浊 |
3.下列有关化学用语表示正确的是( )
| A. | 氯化钠的电子式: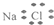 | B. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | ||
| C. | NH3的电子式: | D. | S2-的结构示意图: |
7.在密闭容器中,5mol H2与2mol CO2发生反应:3H2(g)+CO2(g)?CH3OH(g)+H2O(g).反应达到平衡时,改变温度(T)和压强(p),反应混合物中甲醇(CH3OH)的物质的量分数变化情况如图所示.下列说法错误的是( )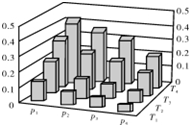

| A. | P1>P2>P3>P4 | |
| B. | 甲醇的物质的量分数越高,反应的平衡常数越大 | |
| C. | 若T1>T2>T3>T4,则该反应为放热反应 | |
| D. | 缩小容积,可以提高CH3OH在混合物中的质量分数 |
17.与C6H6互为同系物的是( )
| A. | C6H5NH2 | B. | C6H5OH | C. | C6H5 CH2OH | D. | C6H5CH2 CH3 |
1.把图2中的物质补充到图1中,可得到一个完整的氧化还原型离子方程式(未配平):

下列关于该离子方程式的说法不正确的是( )

下列关于该离子方程式的说法不正确的是( )
| A. | IO${\;}_{4}^{-}$作氧化剂 | |
| B. | 氧化性:Mn2+>IO${\;}_{3}^{-}$ | |
| C. | 氧化剂与还原剂的物质的量之比为5:2 | |
| D. | 若有2mol Mn2+参加反应,则转移10mol电子 |
 .
. .
.