题目内容
12.美国“海狼”潜艇上的核反应堆内使用了液态铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是( )| A. | 原子半径:Na>Al | |
| B. | 若把铝钠合金投入一定量的水中只得到无色溶液,则n(Al)≤n(Na) | |
| C. | m g不同组成的铝钠合金投入足量盐酸中,若放出H2越多,则铝的质量分数越小 | |
| D. | 铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀生成 |
分析 A.根据同一周期从左到右,元素原子半径逐渐减小;
B.钠和水反应生成的氢氧化钠,足量的氢氧化钠将金属铝溶解;
C.金属钠和金属铝和酸反应生成氢气量的关系:2Al~3H2↑,2Na~H2↑,等质量的金属钠和金属铝,则金属Al产生的氢气量多,所以放出的H2越多,则铝的质量分数越大;
D.铝能与氯化铜溶液反应置换出铜.
解答 解:A.元素周期表中Na、Al位于同周期,Na的原子序数小于Al,故原子半径:Na>Al,故A正确;
B.Na与H2O反应生成NaOH和H2,Al与NaOH反应生成NaAlO2和H2,关系式为Na~NaOH~Al,得到无色溶液,说明Na、Al全部溶解,n(Al)≤n(Na),故B正确;
C.失去1 mol电子(产生$\frac{1}{2}$ mol H2),消耗Na为23 g,而消耗 Al为9 g,故相同质量的Na、Al,后者放出氢气较多,在合金中Al的质量分数越高,放出的氢气就越多,故C错误;
D.铝钠合金投入到足量氯化铜溶液中,钠和水反应2Na+2H2O=2NaOH+H2↑,生成的氢氧化钠可以和氯化铜反应生成氢氧化铜沉淀,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,若n(Al)>n(Na),金属铝也可能会置换出氯化铜中的金属铜,故D正确.
故选C.
点评 本题主要考查了金属的化学性质,把握反应原理及反应与现象的关系为解答的关键,注意从实验的评价性及物质性质分析解答,题目难度不大.

练习册系列答案
相关题目
2.下列反应的离子方程式中,书写正确的是( )
| A. | 硝酸银溶液跟铜反应 Cu+Ag+=Cu2++Ag | |
| B. | 铁粉跟稀盐酸反应 2Fe+6H+=2Fe3++3H2↑ | |
| C. | 钠跟水反应 2 Na+2H2O=2 Na++2OH-+H2↑ | |
| D. | 碳酸钙跟盐酸反应CO32-+2H+=H2O+CO2↑ |
3.一定量的盐酸跟少量的铁粉反应时,为了减缓反应速率但不影响生成H2的总量,可向盐酸中加入( )
| A. | KNO3溶液 | B. | NaCl溶液 | C. | 铜粉 | D. | 硫酸铜晶体 |
20.为验证氧化性:Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和A中的加热装置已略,气密性已经检验完毕)
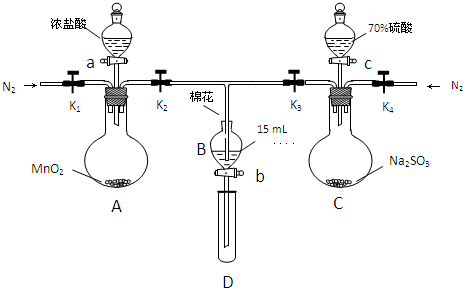
实验过程:
Ⅰ.打开弹簧夹K1-K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4.
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中的溶液变黄时,停止加热,夹紧弹簧夹K2.
Ⅳ.打开活塞b,使约2ml的溶液流入D试管中,检验其中的离子.
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3.
Ⅵ.更新试管D,重复过程IV,检验B溶液中的离子.
(1)过程Ⅰ的目的是排出装置中的氧气
(2)棉花中浸润的溶液为氢氧化钠溶液
(3)A中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O
(4)用70%的硫酸支取SO2,反应速率比用98%的硫酸块,原因是70%的硫酸中的H+的浓度比98%的硫酸中的H+的浓度大
(5)过程Ⅳ中检验B溶液中是否含有硫酸根的操作是取少量B溶液于试管中,加入足量的稀盐酸酸化,在滴加几滴氯化钡溶液,若有白色沉淀生成,证明溶液B中有硫酸根
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化Cl2>Fe3+>SO2的是乙丙
(7)进行实验过程Ⅴ时,B中的溶液颜色由黄色变为红棕色,停止通气,放置一段时间后溶液颜色变为浅绿色.
查阅资料:Fe2+(aq)+SO32-(aq)?FeSO3(s)
提出假设:FeCl3和SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合颜色.
某同学设计如下实验,证实该假设的成立:
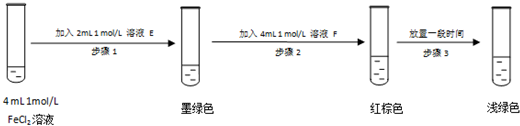
溶液E和F分别是Na2SO3溶液、FeCl3溶液
请用化学平衡原理解释步骤3红棕色溶液变为浅绿色的原因反应2Fe3++SO32-+H2O=2Fe2++SO42-+2H+,促使Fe3++3H2O Fe(OH)3+3H+和SO32-+H2O
Fe(OH)3+3H+和SO32-+H2O  HSO32-+OH-逆向进行,溶液变为浅绿色.
HSO32-+OH-逆向进行,溶液变为浅绿色.

实验过程:
Ⅰ.打开弹簧夹K1-K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4.
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中的溶液变黄时,停止加热,夹紧弹簧夹K2.
Ⅳ.打开活塞b,使约2ml的溶液流入D试管中,检验其中的离子.
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3.
Ⅵ.更新试管D,重复过程IV,检验B溶液中的离子.
(1)过程Ⅰ的目的是排出装置中的氧气
(2)棉花中浸润的溶液为氢氧化钠溶液
(3)A中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O
(4)用70%的硫酸支取SO2,反应速率比用98%的硫酸块,原因是70%的硫酸中的H+的浓度比98%的硫酸中的H+的浓度大
(5)过程Ⅳ中检验B溶液中是否含有硫酸根的操作是取少量B溶液于试管中,加入足量的稀盐酸酸化,在滴加几滴氯化钡溶液,若有白色沉淀生成,证明溶液B中有硫酸根
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化Cl2>Fe3+>SO2的是乙丙
| 过程ⅣB溶液中含有的离子 | 过程ⅥB溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
查阅资料:Fe2+(aq)+SO32-(aq)?FeSO3(s)
提出假设:FeCl3和SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合颜色.
某同学设计如下实验,证实该假设的成立:

溶液E和F分别是Na2SO3溶液、FeCl3溶液
请用化学平衡原理解释步骤3红棕色溶液变为浅绿色的原因反应2Fe3++SO32-+H2O=2Fe2++SO42-+2H+,促使Fe3++3H2O
 Fe(OH)3+3H+和SO32-+H2O
Fe(OH)3+3H+和SO32-+H2O  HSO32-+OH-逆向进行,溶液变为浅绿色.
HSO32-+OH-逆向进行,溶液变为浅绿色.
7.分枝酸可用于生化研究,其结构简式如图.下列关于分枝酸的叙述正确的是( )
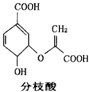

| A. | 可与乙醇、乙酸反应,且反应类型相同 | |
| B. | 1 mo1分枝酸最多可与3 mol NaOH发生中和反应 | |
| C. | 分枝酸的分子式为C10H8O6 | |
| D. | 分枝酸分子中含有2种官能团 |
4.下列关于某些离子的检验说法正确的是( )
| A. | 向某溶液中加稀盐酸,将产生的无色气体通入澄清石灰水中,石灰水变浑浊,则原溶液中一定有CO32-或HCO3- | |
| B. | 向某溶液中加入硝酸钡溶液有白色沉淀产生,再加稀盐酸,沉淀不消失,则原溶液中一定有SO42- | |
| C. | 向某溶液中加入浓氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,则原溶液中存在NH4+ | |
| D. | 分别含有Mg2+、Cu2+、Fe2+和Na+的四种盐溶液,只用NaOH溶液不能一次性鉴别出来 |
1.下列说法正确的是( )
| A. | 离子键就是使阴、阳离子结合成化合物的静电引力 | |
| B. | 在化合物CaCl2中,两个氯离子之间也存在离子键 | |
| C. | 分子中只有共价键的化合物一定是共价化合物 | |
| D. | 不同元素组成的多原子分子中的化学键一定为极性键 |
 .
.