题目内容
15.牛奶放置时间长了会变酸,这是因为牛奶中含有不少乳糖,在微生物的作用下乳糖分解而变成乳酸.乳酸最初就是从酸牛奶中得到并由此而得名的.乳酸的结构简式为 .完成下列问题:
.完成下列问题:(1)一定条件下乳酸能发生的反应类型有BDEF.
A.水解反应 B.取代反应 C.加成反应 D.中和反应 E.氧化反应 F.酯化反应
G.还原反应
(2)写出乳酸与碳酸钠溶液反应的化学方程式:
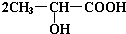 +Na2CO3→
+Na2CO3→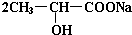 +H2O+CO2↑.
+H2O+CO2↑.(3)乳酸在浓硫酸作用下,两分子相互反应生成链状结构的物质,写出此生成物的结构简式:
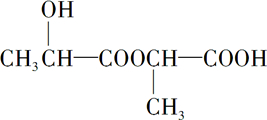 .
.
分析 (1)乳酸中含有醇羟基和羧基,具有醇和羧酸性质;
(2)乳酸中羧基能和碳酸钠反应生成羧酸钠和二氧化碳、水;
(3)乳酸在浓硫酸作催化剂条件下发生酯化反应生成酯.
解答 解:(1)乳酸中含有醇羟基和羧基,具有醇和羧酸性质,能发生取代反应、中和反应、氧化反应、酯化反应,故选BDEF;
(2)羧酸的酸性比碳酸强,碳酸钠能与羧酸反应,不能与醇反应,反应方程式为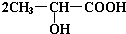 +Na2CO3→
+Na2CO3→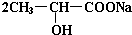 +H2O+CO2↑
+H2O+CO2↑
故答案为: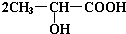 +Na2CO3→
+Na2CO3→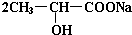 +H2O+CO2↑;
+H2O+CO2↑;
(3)两分子相互反应生成链状结构的物质,为酯,即分子发生酯化反应,该生成物为 ,
,
故答案为: .
.
点评 本题以乳酸的结构为载体,考查官能团的性质,题目难度不大,熟悉常见官能团的性质,进行知识迁移运用即可解答,侧重醇、羧酸性质的考查.

练习册系列答案
相关题目
6.酚酞是中学化学中常用的酸碱指示剂,其结构如图,其含有的饱和碳原子个数为( )
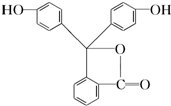

| A. | 1 | B. | 2 | C. | 3 | D. | 5 |
3.以炼锌厂的烟道灰(主要成分为ZnO,另含少量Fe2O3、CuO、SiO2、MnO等)为原料可生产草酸锌晶体(ZnC2O4•2H2O)

有关氢氧化物开始沉淀和沉淀完全的pH如下表:
请问答下列问题:
(1)滤渣A的主要成分为SiO2,滤渣B的主要成分为Fe(OH)3.
(2)除锰过程中产生MnO(OH)2沉淀的离子方程式为Mn2++H2O2+H2O=MnO(OH)2↓+2H+.
(3)①除铁(部分Cu2+可能被除去)时加入ZnO控制反应液pH的范围为3.3~5.4.
②上述流程中除铁与除铜的顺序不能颠倒,否则除铁率会减小,其原因是先加入ZnS会将Fe3+还原为Fe2+,使铁元素难以除去.
(4)沉淀后要获得干燥纯净草酸锌晶体,需进行的操作是过滤、洗涤、干燥.
(5)将草酸锌晶体加热分解可得到一种纳米材料.加热过程中固体残留率随温度的变化如图所示,300℃~460℃范围内,发生反应的化学方程式为ZnC2O4$\frac{\underline{\;△\;}}{\;}$ZnO+CO↑+CO2↑.
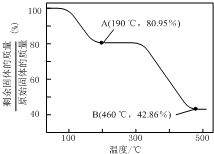

有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 4.2 | 5.4 |
| 沉淀完全的pH | 3.3 | 9.7 | 6.7 | 8.2 |
(1)滤渣A的主要成分为SiO2,滤渣B的主要成分为Fe(OH)3.
(2)除锰过程中产生MnO(OH)2沉淀的离子方程式为Mn2++H2O2+H2O=MnO(OH)2↓+2H+.
(3)①除铁(部分Cu2+可能被除去)时加入ZnO控制反应液pH的范围为3.3~5.4.
②上述流程中除铁与除铜的顺序不能颠倒,否则除铁率会减小,其原因是先加入ZnS会将Fe3+还原为Fe2+,使铁元素难以除去.
(4)沉淀后要获得干燥纯净草酸锌晶体,需进行的操作是过滤、洗涤、干燥.
(5)将草酸锌晶体加热分解可得到一种纳米材料.加热过程中固体残留率随温度的变化如图所示,300℃~460℃范围内,发生反应的化学方程式为ZnC2O4$\frac{\underline{\;△\;}}{\;}$ZnO+CO↑+CO2↑.

10.在C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO的反应中( )
| A. | C作还原剂 | B. | CO2作氧化剂 | ||
| C. | 氧元素化合价降低 | D. | 氧元素化合价升高 |
20.下列物质中既含有离子键又含有共价键的是( )
| A. | Cl2 | B. | NaCl | C. | H2O | D. | NaOH |
4.将金属钠放在燃烧匙中加热使其燃烧,观察到的现象是( )
| A. | 金属钠熔化成小球 | B. | 燃烧后得到白色固体 | ||
| C. | 火焰为黄色 | D. | 燃烧后得到淡黄色固体 |
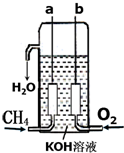 氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制.常用的燃料往往是某些碳氢化合物,如:甲烷、汽油等.已知甲烷燃料电池的负极有碳酸根离子生成,请写出如图所构成的甲烷燃料电池中:a极的电极反应式:CH4+10OH--8e-=CO32-+7H2O,b极的电极反应式:O2+2H2O+4e-=4OH-,若将KOH溶液换为稀H2SO4,则a极的电极反应式:CH4+2H2O-8e-=CO2+8H+.
氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制.常用的燃料往往是某些碳氢化合物,如:甲烷、汽油等.已知甲烷燃料电池的负极有碳酸根离子生成,请写出如图所构成的甲烷燃料电池中:a极的电极反应式:CH4+10OH--8e-=CO32-+7H2O,b极的电极反应式:O2+2H2O+4e-=4OH-,若将KOH溶液换为稀H2SO4,则a极的电极反应式:CH4+2H2O-8e-=CO2+8H+.