题目内容
在温度为830 K时,下列可逆反应及其平衡具有某些特殊性CO+H2O![]() H2+CO2,若起始浓度c(CO)为2 mol·L-1、c(H2O)为3 mol·L-1,反应达平衡时,c(H2)=1.2 mol·L-1;如果c(CO)不变而将H2O的起始浓度加大到6 mol·L-1.则平衡时c(CO)=0.5 mol·L-1.请注意上述有关数据,总结出其中的规律,根据此规律,填写以下空白:
H2+CO2,若起始浓度c(CO)为2 mol·L-1、c(H2O)为3 mol·L-1,反应达平衡时,c(H2)=1.2 mol·L-1;如果c(CO)不变而将H2O的起始浓度加大到6 mol·L-1.则平衡时c(CO)=0.5 mol·L-1.请注意上述有关数据,总结出其中的规律,根据此规律,填写以下空白:
设830 K时,起始浓度c(CO)为a mol·L-1,c(H2O)为b mol·L-1,反应达平衡时c(H2)为c mol·L-1
①当b不变,a减小,重新达平衡时,CO的转化率________,H2O的转化率________(均填“提高”、“降低”或“不变”);
②当a=5,c=![]() 时,b=________;
时,b=________;
③当a=b时,![]() =________;
=________;
④当b=4,c=2时,a=________;
⑤用以表示a、b、c之间关系的代数式:________.
答案:
解析:
提示:
解析:
|
|
提示:
|
利用平衡常数的计算式,得出起始时反应物浓度与平衡浓度的关系,再代入特殊情况下的某些物质的浓度,就可以得出其他物质的浓度. |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 H2+CO2若起始浓度[CO]为2mol/L、[H2O]=
H2+CO2若起始浓度[CO]为2mol/L、[H2O]= 3mol/L,反应达到平衡时,CO的转化率为60%;如果将H2O的起始浓度加大到6mol/L,则CO的转化率为75%。请注意上述有关数据,并总结出规律,完成下列问题:
3mol/L,反应达到平衡时,CO的转化率为60%;如果将H2O的起始浓度加大到6mol/L,则CO的转化率为75%。请注意上述有关数据,并总结出规律,完成下列问题: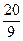 时,b=
时,b= 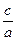 =
=  H2+CO2若起始浓度[CO]为2mol/L、[H2O]= 3mol/L,反应达到平衡时,CO的转化率为60%;如果将H2O的起始浓度加大到6mol/L,则CO的转化率为75%。请注意上述有关数据,并总结出规律,完成下列问题:
H2+CO2若起始浓度[CO]为2mol/L、[H2O]= 3mol/L,反应达到平衡时,CO的转化率为60%;如果将H2O的起始浓度加大到6mol/L,则CO的转化率为75%。请注意上述有关数据,并总结出规律,完成下列问题: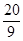 时,b=
时,b=
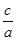 =
=
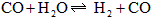 若起始浓度
若起始浓度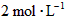 、[
、[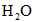 ]为
]为 ,反应达平衡时,
,反应达平衡时,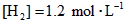 ;如果[CO]不变而将
;如果[CO]不变而将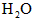 的起始浓度加大到
的起始浓度加大到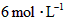 。则平衡时
。则平衡时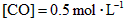 。
。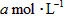 ,[
,[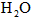 ]为
]为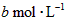 ,反应达平衡时[
,反应达平衡时[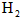 ]为
]为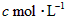
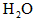 的转化率________(均填“提高”、“降低”或“不变”)
的转化率________(均填“提高”、“降低”或“不变”) 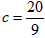 时,b=________;
时,b=________; 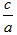 =________;
=________;