题目内容
1.短周期元素X、Y、Z的原子序数依次递增?其原子的最外层电子数之和为13.X与Y、Z位于相邻周期?Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的3倍.下列说法正确的是 ( )| A. | 简单离子半径:Z>Y>X | B. | 氢化物的稳定性:Z>X | ||
| C. | Z的最高价氧化物可用于漂白 | D. | X与Y形成的化合物为离子化合物 |
分析 短周期元素X、Y、Z的原子序数依次递增,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的3倍,则X的内层电子数为2,Z的最外层电子数为6,Y的最外层电子数为2,原子的最外层电子数之和为13,则X的最外层电子数为13-6-2=5,所以X为N,Y为Mg,Z为S,结合元素及其化合物来解答.
解答 解:短周期元素X、Y、Z的原子序数依次递增,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的3倍,则X的内层电子数为2,Z的最外层电子数为6,Y的最外层电子数为2,原子的最外层电子数之和为13,则X的最外层电子数为13-6-2=5,所以X为N,Y为Mg,Z为S,
A.电子层越多,离子半径越大,具有相同电子排布的离子,原子序数大的离子半径小,则离子半径为Z>X>Y,故A错误;
B.X为N、Z为S,氢化物分别为氨气、硫化氢,氨气的稳定性较强,即氢化物的稳定性:Z<X,故B错误;
C.Z为S元素,其最高价氧化物为三氧化硫,三氧化硫不具有漂白性,故C错误;
D.X为N,Y为Mg,二者形成的化合物为氧化镁,MgO为离子化合物,故D正确;
故选D.
点评 本题考查原子结构与元素周期律的关系,题目难度中等,利用原子结构来推断元素是解答本题的关键,注意短周期元素的内层电子只能为2或8,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
12.与HCl比,HI( )
| A. | 颜色更深 | B. | 沸点更低 | C. | 还原性更强 | D. | 稳定性更强 |
13.实验室鉴别己烷、1-己烯和邻二甲苯,可选用的试剂是( )
| A. | 溴水 | B. | 酸性高锰酸钾溶液 | ||
| C. | 氢氧化钠溶液和溴水 | D. | 溴水和酸性高锰酸钾溶液 |
6.Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定,在酸性环境下易分解生成S和SO2.某小组设计了如图实验装置制备Na2S2O3(夹持及加热仪器略),总反应为2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2.回答下列问题:
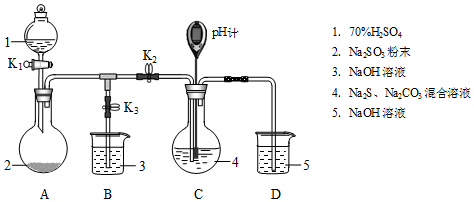
(1)装置A的作用是制备SO2,反应的化学方程式为H2SO4+Na2SO3=SO2↑+H2O+Na2SO4.
(2)完成表实验过程:
(3)Na2S2O3有还原性,可作脱氯剂.向Na2S2O3溶液中通入少量Cl2,某同学预测S2O32-转变为SO42-,设计实验验证该预测:取少量反应后的溶液于试管中,加入过量盐酸,过滤,向滤液中滴加BaCl2溶液,有白色沉淀生成.

(1)装置A的作用是制备SO2,反应的化学方程式为H2SO4+Na2SO3=SO2↑+H2O+Na2SO4.
(2)完成表实验过程:
| 操作步骤 | 装置C的实验现象 | 解释原因 |
| 检查装置气密性后,添加药品 | pH计读数约为13 | 用离子方程式表示(以S2-为例): S2-+H2O?HS-+OH- |
| 打开K2,关闭K3,调节K1使硫酸缓慢匀速滴下 | ⅰ.导管口有气泡冒出,溶液出现淡黄色浑浊,然后逐渐澄清(或浑浊减少); ⅱ.pH计读数逐渐 减小 | 反应分步进行: Na2CO3+SO2═Na2SO3+CO2 2Na2S+3SO2═2Na2SO3+3S↓ Na2SO3+S═Na2S2O3(较慢) |
| 当pH计读数接近7时,立即停止通SO2,操作是关闭K1、K2,打开K3 | / | 必须立即停止通SO2的原因是: SO2过量会使溶液酸度增加,使产物分解,降低产率 |
13.下列反应中氮元素既被氧化又被还原的是( )
| A. | 2NH3+3CuO $\frac{\underline{\;\;△\;\;}}{\;}$N2+3Cu+3H2O | B. | 3NO2+H2O═2HNO3+NO | ||
| C. | 4HNO3(浓)$\frac{\underline{\;光照\;}}{或△}$4NO2↑+O2↑+2H2O | D. | N2+O2 $\frac{\underline{\;放电\;}}{\;}$ 2NO |
10.把1molA和3molB投入2L密闭容器中发生反应A(g)+3B(g)?2C(g)+D(s),2min后,测得C的浓度为0.2mol/L,则下列说法正确的是( )
| A. | v(D)=0.05mol/(L•min) | B. | 3v(B)=2v(C) | ||
| C. | v(B)=0.15mol/(L•min) | D. | A的转化率为40% |
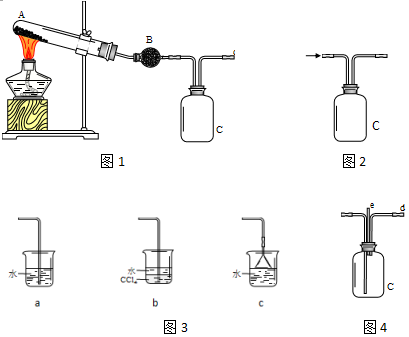
11.如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已 略).

(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.装置 B 中饱和食盐水的作用是;
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中Ⅰ、Ⅱ、Ⅲ依次放入④(填编号)
(3)装置 F 中用足量的 NaOH 溶液吸收余氯,试写出相应的离子方程式2OH-+Cl2=Cl-+ClO-+H2O.
(4)如果将二氧化锰与足量的浓盐酸混合加热,若有17.4g 的 MnO2 被还原,则被氧化的 HCl 的质量为7.3g.
(5)向 Na2CO3 溶液中通入氯气,可制得某种生产和生活中常用于漂白、消毒的 物质,同时有 NaHCO3 生成,该反应的化学方程式是2Na2CO3+Cl2+H2O=2NaHCO3+NaCl+NaClO.

(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.装置 B 中饱和食盐水的作用是;
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中Ⅰ、Ⅱ、Ⅲ依次放入④(填编号)
| ① | ② | ③ | ④ | |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)如果将二氧化锰与足量的浓盐酸混合加热,若有17.4g 的 MnO2 被还原,则被氧化的 HCl 的质量为7.3g.
(5)向 Na2CO3 溶液中通入氯气,可制得某种生产和生活中常用于漂白、消毒的 物质,同时有 NaHCO3 生成,该反应的化学方程式是2Na2CO3+Cl2+H2O=2NaHCO3+NaCl+NaClO.
 某化学兴趣小组用以下装置探究SO2的某些化学性质.
某化学兴趣小组用以下装置探究SO2的某些化学性质.