题目内容
14.在2L密闭恒容容器中投入一定量碳酸镁,在不同的温度下进行反应.MgCO3(s)?MgO(s)+CO2(g)△H,c02的.质的量如下表所示,下列推断不正确的是| 温度 物质的量 时间 | 2min | 4min | 6min | 8min | 10min | 12min |
| 450℃ | 0.2mol | 0.3mol | 0.35mol | 0.40mol | 0.50mol | 0.50mol |
| 480℃ | 0.25mol | 0.35mol | 0.45mol | 0.60mol | 0.60mol | 0.60mol |
| A. | 该反应是熵增,焓增的反应,在较高温度下能自发进行 | |
| B. | 恒温恒压,达到新平衡时,c(CO2)不变,c(MgCO3)增大 | |
| C. | 在2~8min之间CO2平均速率v(CO2)=$\frac{1}{30}$mol•L-1•min-1 | |
| D. | 升高温度,该反应平衡常数、分解速率和MgCO3分解率都增大. |
分析 A、碳酸钙的分解反应生成吸热反应,生成物中产生气体,据此回答;
B、恒温恒压,达到新平衡时,各组分的浓度不随时间的变化而变化,一定温度下,固体的浓度始终是一个常数;
C、在2~8min之间CO2平均速率根据公式v(CO2)=$\frac{△c}{△t}$来计算;
D、吸热反应,升高温度,平衡常数增大,根据温度对反应速率和平衡移动的影响来回答即可.
解答 解:A、碳酸钙的分解反应生成吸热反应,焓增的反应,生成物中产生气体,是熵增反应,根据△H-T△S<0能自发的判据可以得到反应在较高温度下能自发进行,故A正确;
B、恒温恒压,达到新平衡时,各组分的浓度不随时间的变化而变化,一定温度下,固体的浓度始终是一个常数,不会变化,故B错误;
C、450℃,在2~8min之间CO2平均速率v(CO2)=$\frac{△c}{△t}$=$\frac{0.4mol-0.2mol}{2L×6min}$=mol•L-1•min-1,故C错误;
D、反应是吸热反应,升高温度,平衡常数增大,升高温度,反应速率加快,反应正向进行,所以MgCO3分解率增大,故D正确.
故选BC.
点评 本题考查反应的自发性判断、影响反应速率和平衡移动的因素等方面的知识,属于综合知识的考查,难度中等.

练习册系列答案
 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
4.设NA代表阿伏伽德罗常数,下列说法正确的是( )
| A. | 常温常压下,活泼金属从盐酸中置换出1molH2,发生转移的电子数为2NA | |
| B. | 在常温常压下11.2L氯气所含的原子数目为NA | |
| C. | 在1L2mol/L的硝酸镁溶液中含有的硝酸根离子数为4NA | |
| D. | 62gNa2O溶于水后所得溶液中含有O2-离子数为NA |
9.某些含羟基的药物具有苦味,如以下结构的氯霉素:此药物分子中碳链末端羟基(-OH)中的氢原子换成来自棕榈酸中的原子团 后,苦味消失,成为便于口服的无味氯霉素.以下关于无味氯霉素的叙述中正确的是( )
后,苦味消失,成为便于口服的无味氯霉素.以下关于无味氯霉素的叙述中正确的是( )
 后,苦味消失,成为便于口服的无味氯霉素.以下关于无味氯霉素的叙述中正确的是( )
后,苦味消失,成为便于口服的无味氯霉素.以下关于无味氯霉素的叙述中正确的是( )| A. | 它是棕榈酸的酯类 | B. | 它是棕榈酸的盐类 | ||
| C. | 它的水溶性变好,所以苦味消失 | D. | 该过程发生了中和反应 |
19.下列反应在常温下均能自发进行,其中不符合焓判据的是( )
| A. | 2NO(g)+O2(g)═2NO2(g) | |
| B. | Ba(OH)2•8H2O(s)+2NH4Cl(s)═BaCl2(aq)+2NH3•H2O(aq) | |
| C. | 2Na2O2(s)+2CO2(g)═2Na2CO3(s)+O2(g) | |
| D. | 2NO2(g)═N2O4(g) |
6.下列离子组能在溶液中大量共存的是( )
| A. | Mg2+、Fe3+、SO42-、I- | B. | Fe2+、H+、Cl-、NO3- | ||
| C. | Na+、Fe3+、HCO3-、Cl- | D. | Mg2+、Fe3+、SO42-、Cl- |
3.下列各组物质混合后,没有明显现象的是:①H2S和S02;②S02和SO3③SO2和氯水;④S03(气)和C12;⑤H2S和C12( )
| A. | ①③⑤ | B. | ②④ | C. | ②⑤ | D. | ③④⑤ |
15.在恒温下的密闭容器中,有可逆反应N2+3H2?2NH3(该反应放热),不能说明已达到平衡状态的是( )
| A. | 1molN≡N键断裂的同时,有6molN-H键断裂 | |
| B. | 反应器中压强不随时间变化而变化 | |
| C. | v正(NH3)=v逆(H2) | |
| D. | 混合气体平均相对分子质量保持不变 |
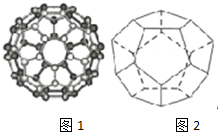 碳是最早被发现和利用的元素之一,长期以来人们以为单质碳的同素异形体只有精钢石、石墨、和无定型碳三种,1985年C60的发现将人类领入认识碳的全新领域--富勒烯,美国科学家Curl和Stnalley教授及英国科学家Kicto教授为此获得了1996年闹贝尔化学奖
碳是最早被发现和利用的元素之一,长期以来人们以为单质碳的同素异形体只有精钢石、石墨、和无定型碳三种,1985年C60的发现将人类领入认识碳的全新领域--富勒烯,美国科学家Curl和Stnalley教授及英国科学家Kicto教授为此获得了1996年闹贝尔化学奖