题目内容
下列表述正确的是( )
A、氢氧根离子的电子式是 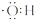 |
B、二氧化碳分子的比例模型是  |
| C、芳香烃的组成通式是CnH2n-6(n≥6) |
D、12C和14C的原子结构示意图均可表示为  |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氢氧根是原子团阴离子,要用中括号括起来,并在右上角表明电荷数;
B.二氧化碳是直线形分子,同一周期元素中,原子直径随着原子序数的增大而减小;
C.CnH2n-6(n≥6)为苯及其同系物的通式,芳香烃没有通式;
D. 表示C元素原子结构示意图,与中子数无关.
表示C元素原子结构示意图,与中子数无关.
B.二氧化碳是直线形分子,同一周期元素中,原子直径随着原子序数的增大而减小;
C.CnH2n-6(n≥6)为苯及其同系物的通式,芳香烃没有通式;
D.
 表示C元素原子结构示意图,与中子数无关.
表示C元素原子结构示意图,与中子数无关.解答:
解:A.氢氧根是原子团阴离子,要用中括号括起来,并在右上角表明电荷数,因氧原子最外层6个电子,氢原子最外层1个电子,则OH-的电子式为 ,故A错误;
,故A错误;
B.二氧化碳是直线形分子,同一周期元素中,原子直径随着原子序数的增大而减小,则二氧化碳分子正确的比例模型为: ,故B错误;
,故B错误;
C.含有苯环的烃都属于芳香烃,所以芳香烃没有通式,故C错误;
D.12C和14C的质子数都是6,其原子结构示意图相同,都可以表示为: ,故D正确;
,故D正确;
故选D.
 ,故A错误;
,故A错误;B.二氧化碳是直线形分子,同一周期元素中,原子直径随着原子序数的增大而减小,则二氧化碳分子正确的比例模型为:
 ,故B错误;
,故B错误;C.含有苯环的烃都属于芳香烃,所以芳香烃没有通式,故C错误;
D.12C和14C的质子数都是6,其原子结构示意图相同,都可以表示为:
 ,故D正确;
,故D正确;故选D.
点评:本题考查了常见化学用语的判断,题目难度中等,注意掌握原子结构示意图、比例模型与球棍模型、电子式等化学用语的表示方法,明确球棍模型与比例模型、羟基与氢氧根离子的电子式的区别,试题培养了学生规范答题的能力.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案
相关题目
常温下,下列溶液中的微粒浓度关系正确的是( )
| A、pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) |
| B、0.4 mol?L-1 CH3COOH溶液与0.2 mol?L-1 NaOH溶液等体积混合:2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-) |
| C、氯水中加入少许NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) |
| D、NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
下列措施能明显增大原反应的化学反应速率的是( )
| A、Na与水反应时增大水的用量 |
| B、将稀H2SO4改为98%的浓H2SO4与Zn反应制取H2 |
| C、在H2SO4与NaOH两溶液反应时,增大压强 |
| D、恒温恒容条件下,在工业合成氨反应中,增加氮气的量 |
设NA表示阿伏加德罗常数的值,下列表述不正确的是( )
| A、标准状况下,22.4L氢气所含原子数是2NA |
| B、5.4g水所含的分子数为0.3NA |
| C、1mol金属钠与水反应失去的电子数为NA |
| D、物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA |
设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A、标准状况下,11.2 L NO和11.2 L SO3的分子总数为0.5NA |
| B、0.1molBr2与足量H2O或NaOH反应转移的电子数均为0.1NA |
| C、0.1mol的白磷(P4)或四氯化碳(CCl4)中所含的共价键数均为0.4NA |
| D、在精炼铜或电镀铜的过程中,当阴极析出铜32g转移电子数均为NA |