题目内容
实验室制Cl2反应为4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O下列说法不正确的是
MnCl2+Cl2↑+2H2O下列说法不正确的是
A.还原剂是浓HCl,氧化剂是MnO2
B.每生成1mol Cl2,转移电子2mol
C.每消耗1mol MnO2,浓HCl被还原4mol
D.转移1mol电子时,生成的Cl2在标准状况下体积为11.2 L
C
【解析】
试题分析:浓盐酸中的氯离子生成氯气单质,价态由-1价升高到0价,作还原剂,二氧化锰生成氯化锰,价态由+4价降低到+2价,做氧化剂,A正确;每生成1molCl2,转移2mol电子,B正确;每消耗1molMnO2,转移2mol电子,被氧化的盐酸为2mol,C错误;转移1mol电子时,生成的Cl2的物质的量为0.5mol,在标准状况下体积为11.2L,D正确;答案选C.
考点:氧化还原反应

 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案(18分)C、O、Na、Al、S、Cl是常见的六种元素
(1)C元素位于元素周期表第 周期,第 族;C元素的一种同位素可以测定文物年代,这种同位素的符号为
(2)用“大于”“小于”或“等于”填空
离子半径 | 还原性 | 得电子能力 |
N3- Al3+ | O2- S2- | 35Cl 37Cl |
(3)① CaCO3和适量HCl溶液反应时,每产生4.4 g 气体(不考虑气体溶解),放热a kJ,则该反应的热化学方程式为 。
②上述反应至无气泡逸出后,取适量残留溶液,插入pH传感器并逐滴滴入碳酸钠溶液,测得pH变化曲线如图所示


请用离子方程式表示B-C段发生的反应:
(4)氢气、氧气常用来作燃料电池,写出电解质为氢氧化钠溶液时负极上的电极方程式
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
阳离子 | Ag+、Na+ |
阴离子 | NO3—、SO42—、Cl- |
下图Ⅰ所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了27 g。常温下各烧杯中溶液的pH与电解时间t的关系如下图Ⅱ所示。据此回答下列问题:
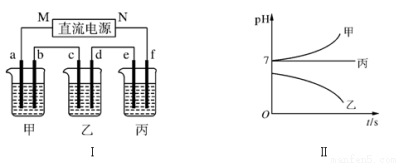
(1)M为电源的________(填“正”或“负”)极,A是________(填写化学式)。
(2)计算电极f上生成的气体在标准状况下的体积:________。
(3)写出乙烧杯的电解池反应:________________________________________________。
(4)要使丙恢复到原来的状态,应加入________ g ________(填写化学式)。
 Na++ HSO4-
Na++ HSO4-